Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

HD:
Gọi M là kim loại trung bình của 2 kim loại cần tìm. Ta có:
M + H2SO4 ---> MSO4 + H2
2 98x 8,72 2x
Gọi x là số mol M phản ứng. Áp dụng định luật bảo toàn khối lượng ta có: 2 + 98x = 8,72 + 2x. Suy ra x = 0,07 mol.
Như vậy, khối lượng trung bình của kim loại M = 2/0,07 = 28,57. Vì hai kim loại ở nhóm IIA mà thuộc 2 chu kỳ liên tiếp nên hai kim loại đó là Mg và Ca.

Đáp án: A
Ta có: nHCl= 2nH2 = 0,5 mol
m muối = m kim loại + mCl-
= 8,4 + 0,5. 35,5 = 26,15 gam

\(CT:\overline{M}_2CO_3\)
\(n_{CO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\overline{M}_2CO_3+2HCl\rightarrow2\overline{M}Cl+CO_2+H_2O\)
\(.............0.2..............0.1.....0.1\)
\(m_{HCl}=0.2\cdot36.5=7.3\left(g\right)\)
\(m_{CO_2}=0.1\cdot44=4.4\left(g\right)\)
\(m_{H_2O}=0.1\cdot18=1.8\left(g\right)\)
\(BTKL:m_{hh}+m_{HCl}=m_{Muối}+m_{CO_2}+m_{H_2O}\)
\(\Leftrightarrow8.9+7.3=m_{Muối}+4.4+1.8\)
\(\Leftrightarrow m_{muối}=8.9+7.3-4.4-1.8=10\left(g\right)\)

Đáp án B.
Gọi công thức chung của hai kim loại là X
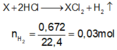
![]()
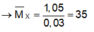
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg

Vì hai kim loại đều thuộc nhóm IIA nên đặt công thức chung của hỗn hợp kim loại là là X ¯ ( X ¯ có hóa trị II không đổi).
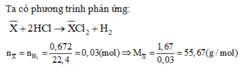
Do đó trong hỗn hợp có 1 kim loại có khối lượng mol nhỏ hơn 55,67 và 1 kim loại có khối lượng mol lớn hơn 55,67.
Mặt khác hai kim loại này thuộc hai chu kì liên tiếp.
Nên 2 kim loại cần tìm là Ca và Sr.
Đáp án D.




Ap dụng tăng giảm khối lượng
\(n_{MCO_3}=\frac{20,6-18,4}{35,5.2-60}=0,2\)
\(M+60=18,4:0,2=92\Leftrightarrow M=32\)suy ra 2 nguyên tố đó là Mg và Ca