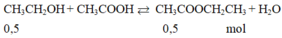Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nC2H5OH = 8.05/46 = 0.175 (mol)
nCH3COOH = 36/60 = 0.6 (mol)
nCH3COOC2H5 = 12.32/88 = 0.14 (mol)
C2H5OH + CH3COOH <-H2SO4đ,t0-> CH3COOC2H5 + H2O
1.......................1
0.175................0.6
LTL : 0.175/1 < 0.6/1
=> CH3COOH dư
mCH3COOH (dư) = ( 0.6 - 0.175) * 60 = 25.5 (g)
nCH3COOC2H5 = nC2H5OH = 0.175 (mol)
H% = 0.14/0.175 * 100% = 80%

PTHH: \(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\) (1)
\(2CH_3COOH+2Na\rightarrow2CH_3COONa+H_2\) (2)
a) Ta có: \(n_{H_2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Đặt số mol của \(C_2H_5OH\) là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=\frac{1}{2}a\)
Đặt số mol của \(CH_3COOH\) là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=\frac{1}{2}b\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}46a+60b=20,5\\\frac{1}{2}a+\frac{1}{2}b=0,2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,25\\b=0,15\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_5OH}=0,25mol\\n_{CH_3COOH}=0,15mol\end{matrix}\right.\)
\(\Rightarrow m_{CH_3COOH}=60\cdot0,15=9\left(g\right)\)
\(\Rightarrow\%m_{CH_3COOH}=\frac{9}{20,5}\cdot100\approx43,9\%\)
\(\Rightarrow\%m_{C_2H_5OH}=56,1\%\)
b) PTHH: \(C_2H_5OH+CH_3COOH\underrightarrow{xt}CH_3COOC_2H_5+H_2O\)
Xét tỷ lệ: \(\frac{0,15}{1}< \frac{0,25}{1}\) \(\Rightarrow\) Axit phản ứng hết, Rượu còn dư
\(\Rightarrow n_{CH_3COOC_2H_5}=0,15mol\) \(\Rightarrow m_{este}=0,15\cdot88=13,2\left(g\right)\)
\(\Rightarrow m_{este}thực=13,2\cdot90\%=11,88\left(g\right)\)

Đáp án: C
n C H 3 C O O H = 180 60 = 3 m o l ; n C 2 H 5 O H = 138 46 = 3 m o l
n C H 3 C O O H phản ứng = 3.44% = 1,32 mol
PTHH: C H 3 C O O H + C 2 H 5 O H C H 3 C O O C 2 H 5 + H 2 O
Ban đầu: 3 mol 3 mol 0
Phản ứng: 1,32 mol → 1,32 mol → 1,32 mol
=> Khối lượng este thu được là: 1,32.88 = 116,16 (gam)