Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Do R thuộc nhóm IIA nên R có hóa trị II.
PT: \(R+2HCl\rightarrow RCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_R=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{9,6}{0,4}=24\left(g/mol\right)\)
Vậy: R là Magie (Mg).
Bạn tham khảo nhé!

8,96l Cl2 + H2 ---H=75%---> 2HCl
0,4............................................0,8
V Hcl lí thuyết : 0,8 . 22,4 = 17,92 (l)
V HCl thực tế : 17,92 . 75% = 13,44 (l)
\(n_{Cl_2}=\dfrac{8,96}{22,4}=0,25\left(mol\right)\)
PT: Cl2 + H2 → 2HCl
Mol: 0,25 0,5
\(m_{HCl\left(lt\right)}=0,5.36,5=18,25\left(g\right)\)
\(\Rightarrow m_{HCl\left(tt\right)}=75\%.18,25=13,6875\left(g\right)\)

\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ n_{Cl_2}=\dfrac{V_{Cl_2\left(ĐKTC\right)}}{22,4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:2Al+3Cl_2\rightarrow2AlCl_3\\ \dfrac{n_{Al}}{n_{Cl_2}}=\dfrac{1}{2}< \dfrac{2}{3}\Rightarrow Cl_2\text{ dư, bài toán tính theo }Al\\ \Rightarrow m_{AlCl_3}=n_{AlCl_3}\cdot M_{AlCl_3}=0,2\cdot133,5=26,7\left(g\right)\)

\(n_{AgCl}=\dfrac{43.05}{143.5}=0.3\left(mol\right)\) \(\Rightarrow n_{HCl}=0.3\left(mol\right)\)
\(n_{HCl}=\dfrac{6.72}{22.4}=0.3\left(mol\right),n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{^{^{t^0}}}2HCl\)
\(0.15....0.15.......0.3\)
\(H\%=\dfrac{0.15}{0.2}\cdot100\%=75\%\)

\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)

- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)

Đáp án D
Xét trường hợp 20,4 gam A tác dụng với dung dịch HCl dư:
Gọi số mol các chất là Al: a mol; Zn: b mol; Fe: c mol
Ta có:

Các quá trình nhường, nhận electron:
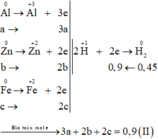
Xét trường hợp 0,2 mol A tác dụng với Cl2:
Gọi số mol các chất là Al: ka mol; Zn: kb mol; Fe: kc mol
Ta có:
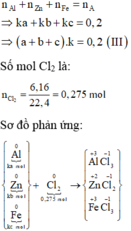
Các quá trình nhường, nhận electron:
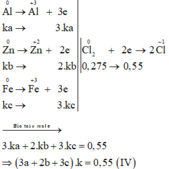
Lấy (IV) chia (III) vế với vế ta được:


Gọi a và b lần lượt là số mol của Cu và Zn
Bảo toàn khối lượng: \(m_{Cl_2}=m_{muối}-m_{hh}=8,52\left(g\right)\)
\(\Rightarrow n_{Cl_2}=\dfrac{8,52}{71}=0,12\left(mol\right)\)
Bảo toàn mol e: \(2a+2b=0,24\)
Mà \(64a+65b=7,75\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,07\end{matrix}\right.\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Theo PTHH: \(n_{H_2}=n_{Zn}=0,07mol\)
\(\Rightarrow V_{H_2}=0,07\cdot22,4=1,568\left(l\right)\)
\(n_{H_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(n_{Cl_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{AS}HCl\)
\(0.4.......0.4.........0.4\)
\(V_{HCl}=0.4\cdot22.4=8.96\left(l\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
PT: \(Cl_2+H_2\underrightarrow{t^o,as}2HCl\)
Ta có: \(n_{Cl_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}>\dfrac{0,4}{1}\) , ta được Cl2 dư.
Theo PT: \(n_{HCl}=2n_{H_2}=0,8\left(mol\right)\)
Không biết đề bài yêu cầu tính thể tích hay khối lượng HCl bạn nhỉ?