Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Gọi x, y, z 1à số mol của CH4, C2H4 và C2H2 trong 8,6g hh X
=> 16x + 28y + 26z = 8,6 (1)
- Khi cho X td với dung dịch Br2 dư:
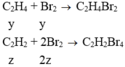
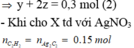


Khối lượng sắt:mFe=0,46298*60,5=28 g=>mZn=32,5g
=>nFe=0,5;nZn=0,5
ta có:nCl- =2nFe+2nZn=2 mol =>nHCl=2mol
=>nH2 =1mol.=>V H2=44,8 lit
m muối =m kim loại +m Cl- =60,5 +2*35,5=131,5

Chọn B.
Nhận thấy MY = 13,2 Þ Y có chứa H2 dư. Khi đó Y gồm C2H6: 0,2 mol và H2 dư: 0,3 mol
Vì C2H2, C2H4 có cùng số mol Þ mol mỗi chất bằng 0,1 mol
Khi dẫn X qua dung dịch Br2 thì: mb.tăng = mhiđrocacbon = 5,4 (g)

Đáp án C
Gọi số mol CH4, C2H4, C2H2 lần lượt là a, b, c => 16a+28b+26c= 8,6
Cho 8,6 gam X tác dụng vừa đủ với 0,3 mol Br2 => b+2c= 0,3
Mặt khác 0,6 mol X tác dụng với AgNO3/NH3 thu được 36 gam kết tủa AgC≡CAg
→ n A g 2 C 2 = 0 , 15 m o l → c a + b + c = 0 , 15 0 , 6
Giải hệ: a=0,2; b=0,1; c=0,1 nên % V C H 4 =50%.

Gọi số mol của CH4 , C2H4 , C2H2 lần lượt là x , y , z
Ta có 16x + 28y + 26z = 8,6 (1)
t/d với Br: C2H4 + Br2 y--------> y
C2H2 + 2Br2
z --------> 2z => y + 2z = 0,3 (2) 0,6 mol X t/d AgNO3 trong NH3
C2H2 ------> C2Ag2
0,15 < ------ 0,15 Lập luận:
0,6 mol X t/d AgNO3 trong NH3 ----------> 0,15 mol kết tủa
8,6 g X ( tương ứng x + y + z mol ) t/ AgNO3 trong NH3 --------> z mol kết tủa ( n kết tủa = z)
=> 0,6 / ( x + y + z) = 0,15 /z <=> x + y - 3z = 0 (3) Từ (1) (2) (3) giải hệ => nCH4 = 0,3 => %CH4 = 50%
=> Đáp án A
