Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 61- Nước là hợp chất gồm nguyên tố Hiđro và nguyên tố Oxi, chúng hóa hợp với nhau theo tỉ lệ thể tích là:
A/ 1 phần khí hiđro, 2phần khí oxi B/ 2 phần khí hiđro, 1 phần khí oxi
C/ 1phần khí hiđro, 8phần khí oxi D/ 8phần khí hiđro, 1 phần khí oxiCâu 62- Dãy chất nào chỉ gồm các Bazơ?
A/ H2SO4, HNO2, NaOH B/ Ba(OH)2, Al(OH)3, LiOH
C/ H2SO4, H2S, HCl D/ HCl, NaOH, CuO
Câu 63: Một oxit của kim loại R (hoá trị II ). Trong đó kim loại R chiếm 71,43% theokhối lượng. Công thức của oxit là: A. FeO B. MgO C. CaO D. ZnO
Câu 64: Lưu huỳnh đi oxit (SO2) tác dụng được với các chất trong dãy hợp chất nào sau đây:
A. H2O, NaOH, CaO B. H2O, H2SO4, CO2
C. HCl, H2SO4, K2O D. H2O, H2SO4, Ba(OH)2
Câu 65: Cho 3 hợp chất oxit : CuO, Al2O3, K2O. Để phân biệt 3 chất trên ta dùng chất nào sau đây làm thuốc thử ?A. Nước cất B. Dùng axit HCl C. Dùng dung dịch NaOH D. Dung dịch KOH
Câu 66: Để hòa tan hoàn toàn 1,3g kẽm thì cần 14,7g dung dịch H2SO4 20%. Khi phản ứng kết thúc khối lượng hiđro thu được là:
A. 0,03g B. 0,04g C. 0,05g D. 0,06g
Câu 67: Khí SO2 được tạo thành từ cặp chất nào sau đây ?
A. K2SO3 và H2SO4 B. Na2SO4 và CuCl2
C. Na2SO3 và NaOH D. Na2SO3 và NaCl
Câu 68: Khí O2 bị lẫn tạp chất là các khí CO2, SO2, H2S. Có thể dùng chất nào sau đây để loại bỏ tạp chất:
A. Dung dịch H2SO4 loãng B. Dung dịch CuSO4 C. Dung dịch Ca(OH)2 D. Nước
Câu 69: Hòa tan 5 gam một kim loại R (chưa rõ hóa trị ) cần vừa đủ 36,5 gam dung dịch HCl 25%. Kim loại R là:A. Mg B. Fe C. Ca D. Zn
Câu 70: Cho 10,5 gam hỗn hợp hai kim loại Zn, Cu vào dung dịch H2SO4 loãng dư, thu được 2,24 lít khí(đktc). Phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu là:
A. 61,9% và 38,1% B. 50% và 50% C. 40% và 60% D. 30% và70%
Câu 71: Oxit là loại hợp chất được tạo thành từ:
A. Một phi kim và một kim loại B. Một kim loại và một hợp chất khác
C. Một phi kim và một hợp chất khác D. Một nguyên tố khác và oxi
Câu 72: Để trung hòa 44,8 gam dung dịch KOH 25% thì khối lượng dung dịch HCl 2,5% là:
A. 310 gam B. 270 gam C. 292 gam D. 275 gam
Câu 73: Hòa tan hoàn toàn 7,8 gam một kim loại hóa trị I vào nước được một dung dịch bazơ X và 2,24 lít H2 (đktc). Tên kim loại hóa trị I là:
A. Natri. B. Bạc. C. Đồng. D. Kali.
Câu 74: Oxit là
A. Hỗn hợp của nguyên tố oxi với một nguyên tố hoá học khác.
B. Hợp chất của nguyên tố phi kim với một nguyên tố hoá học khác.
C. Hợp chất của oxi với một nguyên tố hoá học khác.
D. Hợp chất của nguyên tố kim loại với một nguyên tố hoá học khác.
Câu 75: Oxit axit là: A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với dung dịch bazơ và dung dịch axit.
D. Những oxit chỉ tác dụng được với muối.
Câu 76: Oxit Bazơ là: A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với dung dịch bazơ và dung dịch axit.
D. Những oxit chỉ tác dụng được với muối.
Câu 77: Oxit lưỡng tính là: A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ và tác dụng với dung dịch axit tạo thành muối và nước.
C. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.D. Những oxit chỉ tác dụng được với muối.

\(2A+nCI2\rightarrow2ACIn\)
\(nA=\frac{1.96}{M}\)
\(nACI2=\frac{5,6875}{\left(M+35,5n\right)}\)
\(nA=nACI2\)
\(\Rightarrow\frac{1,96}{M}=\frac{5,6875}{\left(M+35,5n\right)}\)
\(\Rightarrow M=\frac{56}{3n}\)
\(\Rightarrow n=1\) \(M=\frac{56}{3}\left(Loại\right)\)
\(n=2\) \(M=\frac{112}{3}\left(Loại\right)\)
\(n=3\) \(M=56\)
Vậy A là Fe
\(Fe+HCI\rightarrow FeCI2+H2\)
\(FexOy+\frac{HCI\rightarrow FeCI2y}{x+H2O}\)
\(FexOy+H2\rightarrow Fe+H2O\)
Goi a b lần lượt là số mol của Fe và FexOy trong 4,6 gam hỗn hợp
\(nFe=a\Rightarrow nHCI=2a\)
\(nFexOy=b\Rightarrow nHCI=2by\)
\(nHCI=0,08\cdot2=1,6mol\)
\(\Rightarrow2a+2by=0,16\)
\(\Rightarrow a+by=0,08\left(1\right)\)
\(56a+b\left(56x+16y\right)=4,6\Rightarrow56a+56bx+16by=4,6\left(2\right)\)
Chất rắn X là Fe
\(nFexOy=b\)
=> nFe sinh ra là bx
\(\Rightarrow56a+56bx=3,64\left(3\right)\)
Từ (1) (2) và (3) ta có hệ:
\(\begin{cases}a+by=0,08\\56a+56bx+16by=4,6\\56a+56bx=3,64\end{cases}\)
\(a=0,02\\
bx=0,045\\
by=0,06\)
\(\frac{\Rightarrow bx}{by}=\frac{x}{y}=\frac{0,045}{0,06}=\frac{3}{4}\)
=> Công thức của oxit cần tìm là: Fe3O4
2A+nCl2 -------------->2ACln
nA=1.96/M
nACl2=5,6875/(M+35,5n)
nA=nACl2
=> 1,96/M=5,6875/(M+35,5n)
=>M=56/3n
=> n=1 M=56/3 (Loại)
n=2 M=112/3 (Loại)
n=3 M=56
Vậy A là Fe
Fe+HCl--->FeCl2+H2
FexOy+HCl---->FeCl2y/x+H2O
FexOy+H2---->Fe+H2O
Goi a b lần lượt là số mol của Fe và FexOy trong 4,6 gam hỗn hợp
nFe=a=>nHCl=2a
nFexOy=b=>nHcl=2by
nHCl=0,08*2=1,6 mol
=> 2a+2by=0,16
=> a+by=0,08 (1)
56a+b(56x+16y)=4,6=> 56a+56bx+16by=4,6 (2)
Chất rắn X là Fe
nFexOy=b
=> nFe sinh ra là bx
=> 56a+56bx=3,64 (3)
Từ (1) (2) và (3) ta có hệ:
{a+by=0,08
{56a+56bx+16by=4,6
{56a+56bx=3,64
a=0,02
bx=0,045
by=0,06
=> bx/by=x/y=0,045/0,06=3/4
=> Công thức của oxit cần tìm là: Fe3O4

Câu 78 Oxit trung tính là: A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với axit, bazơ, nước.
D. Những oxit chỉ tác dụng được với muối
Câu 79: Chất tác dụng với nước tạo ra dung dịch bazơ là:
A. CO2, B. Na2O. C. SO2, D. P2O5
Câu 80 Chất tác dụng với nước tạo ra dung dịch axit là
A. K2O. B. CuO. C. P2O5. D. CaO.

1/ Ta thấy 6,72 lít H2 ở đktc là sản phẩm của Al với HCl ( vì Ag không pứ với HCl)
PTHH: 2Al + 6HCl ===> 2AlCl3 + 3H2
nH2 = 6,72 / 22,4 = 0,3 mol
=> nAl = 0,2 mol
=> mAl = 0,2 x 27 = 5,4 gam
CHất rắn không tan chính là Ag
Tính phẩn trăm thì bạn tự tính nhé!
2/ Gọi hóa trị của R là x
PTHH: 2R + 2xHCl ===> 2RClx + xH2
nH2 = 1,008 / 22,4 = 0,045 mol
=> nR = \(\frac{0,045.2}{x}\) = 0,09 / x (mol)
=> MR = 25,2 : \(\frac{0,09}{x}\) = 280x
?????? Mình cũng không biết!! Chắc đề sai rồi bạn ạ!

a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

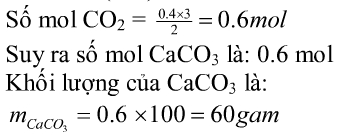
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g

Kl Oxi: m(O) = [m(0xit) - m(Kim loai)] = (22,3 - 14,3) = 8
====> n(0) = 8/16 = 0,5(m0l)
Theo bảo toàn nguyên tố ta có:
+, n(H20) = n(0) = 0,5 (mol)
+, n(HCl) = 2n(H20) = 0,5*2 = 1 (m0l)
Theo bảo toàn khối lượng:
m(Oxit) + m(Axit) = m(Muối) + m(Nước)
=====> m(Muối) = m(0xit) + m(Axit) - m(H20) = 22,3 + 36,5*1 - 18*0,5 = 49,8

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 → M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ---> 2Al + 3/2O2
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O ---> 2Al(OH)3 + 3Na2SO4 + 3CO2

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 --->M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ------> 2Al + 3/2O2
Al2O3 + 2NaOH --->2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O --->2Al(OH)3+ 3Na2SO4 + 3CO2

Câu 81:Chất tác dụng với nước tạo ra dung dịch bazơ là:
A. K2O. B. CuO. C. CO. D. SO2.
Câu 82 Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO, B. BaO, C. Na2O D. SO3
Câu 83 Hòa tan hết 12,4 gam Natrioxit vào nước thu được 500ml dung dịch A . Nồng độ mol của dung dịch A là A. 0,8M B. 0,6M C. 0,4M D. 0,2M
Câu 84 Để nhận biết 2 lọ mất nhãn đựng CaO và MgO ta dùng:
A. HCl B. NaOH C. HNO3 D. Quỳ tím ẩm
Câu 85 Chất nào dưới đây có phần trăm khối lượng của oxi lớn nhất ?
A. CuO B. SO2 C. SO3 D. Al2O3
Câu 86 Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Khối lượng dung dịch HCl đã dùng
A. 50 gam B. 40 gam C. 60 gam D. 73 gam
Câu 87 Cặp chất tác dụng với nhau sẽ tạo ra khí lưu huỳnh đioxit là:
A. CaCO3 và HCl B. Na2SO3 và H2SO4 C. CuCl2 và KOH D. K2CO3 và HNO3
Câu 88 Oxit của một nguyên tố hóa trị (II) chứa 28,57% oxi về khối lượng . Nguyên tố đó là:
A. Ca B. Mg C. Fe D. C
Câu 89 Cho 2,24 lít CO2 (đktc) tác dụng với dung dịch Ba(OH)2 dư. Khối lượng chất kết tủa thu được là :
A. 19,7 g B. 19,5 g C. 19,3 g D. 19 g
Câu 90 Khí có tỉ khối đối với hiđro bằng 32 là:
A. N2O B. SO2 C. SO3 D. CO2
Câu 91 Hòa tan 12,6 gam natrisunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc là:
A. 2,24 lít B. 3,36 lit C. 1,12 lít D. 4,48 lít
Câu 92: Hòa tan hoàn toàn 29,4 gam đồng(II)hidroxit bằng dd axit sunfuric.Số gam muối thu được sau phản ứng:
A. 48gam B. 9,6gam C. 4,8gam D. 24gam
Câu 93: Ở 200C, độ tan của dung dịch muối ăn là 36g. Nồng độ % của dung dịch muối ăn bảo hoà ở 200C:
A. 25,47% B. 22,32% C. 25% D. 26,47%
Câu 94: Nồng độ mol/lít của dung dịch cho biết:
A. Số mol chất tan có trong 1 lít dung dịch bão hoà.
B. Số mol chất tan có trong 1 lít dung dịch.
C. số gam chất tan có trong 1 lít dung dịch
D. Số mol chất tan có trong 1 lít dung môi
Câu 95: Một oxit có công thức Mn2Ox có phân tử khối là 222. Hoá trị của Mn trong oxit trên là: 7

Gọi CTHH oxit sắt cần tìm là \(Fe_xO_y\)
\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)
\(n_{FeCl_{\dfrac{2y}{x}}}=x.n_{Fe_xO_y}\\ \Leftrightarrow\dfrac{12,7}{56+35,5\cdot\dfrac{2x}{y}}=\dfrac{7,2x}{56x+16y}\\ \Leftrightarrow308x=308y\\ \Rightarrow\dfrac{x}{y}=\dfrac{308}{308}=\dfrac{1}{1}\)
CTHH oxit sắt cần tìm là \(FeO\)