Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) Phải rót từ từ axit đặc vào nước , khuấy đều bằng đũa thủy tinh. => Chọn D
Vì axit đặc rất háo nước , khi rót nước vào axit , nước sôi đột ngột kéo theo axit bắn ra gây nguy hiểm.
2) CuO + H2SO4 --> CuSO4 + H2O
dụng dịch CuSO4 có màu xanh làm => Chọn D
Câu D
Muốn pha loãng axit sunfuric đặc người ta phải rót từ từ axit đặc vào nước

(1) Al2(SO4)3
(2) NaOH
(3) BaCl2
(4) Na2SO4
(5) (CH3COO)2Ca
* \(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4\downarrow\)
* \(6NaOH+Al_2\left(SO_4\right)_3\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\downarrow\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
* \(\left(CH_3COO\right)_2Ca+Na_2SO_4\rightarrow CaSO_4\downarrow+2CH_3COONa\)

Có 5 lọ: Na2SO4, (CH3COO)2Ba, Al2(SO4)3, NaOH và Ba(OH)2
Rót từ từ các chất từ lọ này vào lọ khác ta có bảng sau:

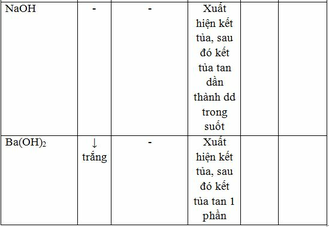
Dấu ‘ – ‘ thể hiện không có phản ứng xảy ra.
Từ giả thiết bài toán:
- Rót dung dịch từ lọ (4) vào lọ (3) hoặc (5) đều tạo kết tủa => lọ (4) có thể là Na2SO4 hoặc (CH3COO)2Ba vì từ bảng ta thấy 2 chất này cùng tạo 2 kết tủa với các chất khác.
- Rót từ từ đến dư dd trong lọ (2) vào lọ (1) thì có kết tủa sau đó kết tủa tan dần tạo thành dung dịch trong suốt => lọ (2) là NaOH; lọ (1) là Al2(SO4)3
- Rót từ từ đến dư dd lọ (5) vào lọ (1) thì có kết tủa sau đó kết tủa tan một phần => lọ (5) là Ba(OH)2 và lọ (1) là Al2(SO4)3.
- Từ lọ (5) là Ba(OH)2 => lọ (4) là Na2SO4 => lọ (3) là (CH3COO)2Ba
Kết luận: Vậy thứ tự các lọ là:
(1) Al2(SO4)3
(2) NaOH
(3) (CH3COO)2Ba
(4) Na2SO4
(5) Ba(OH)2
Các phản ứng hóa học xảy ra:
Na2SO4 + (CH3COO)2Ba → BaSO4↓ + 2CH3COONa
Na2SO4 + Ba(OH)2 → BaSO4↓ + 2NaOH
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4
NaOH dư + Al(OH)3↓ → NaAlO2 + 2H2O
Ba(OH)2 + Al2(SO4)3 → 2Al(OH)3↓ + 3BaSO4↓ (không tan khi cho Ba(OH)2 dư)
Ba(OH)2 + 2Al(OH)3↓ → Ba(AlO2)2 + 4H2O

Khi axit sunfuric gặp nước thì lập tức sẽ có phản ứng hóa học xảy ra, đồng thời sẽ tỏa ra một nhiệt lượng lớn. Axit sunfuric đặc giống như dầu và nặng hơn trong nước. Nếu bạn cho nước vào axit, nước sẽ nổi trên bề mặt axit. Khi xảy ra phản ứng hóa học, nước sôi mãnh liệt và bắn tung tóe gây nguy hiểm.
Trái lại khi bạn cho axit sunfuric vào nước thì tình hình sẽ khác: axit sunfuric đặc nặng hơn nước, nếu cho từ từ axit vào nước, nó sẽ chìm xuống đáy nước, sau đó phân bố đều trong toàn bộ dung dịch. Như vậy khi có phản ứng xảy ra, nhiệt lượng sinh ra được phân bố đều trong dung dịch, nhiệt độ sẽ tăng từ từ không làm cho nước sôi lên một cách quá nhanh.

a) Axit axetic là chất lỏng, không màu, vị chua, tan nhiều trong nước.
b) Axit axetic là nguyên liệu điều chế các loại tơ,phẩm nhuộm,...
c) Giấm ăn là dung dịch axit axetic có nồng độ từ 2 đến 5%
d) Bằng cách oxi hóa không hoàn toàn butan với chất xúc tác thích hợp người ta thu được axit axetic

Câu 5 :
Phương pháp : Cho từ từ dung dịch $H_2SO_4$ đặc vào nước. Tuyệt đối không làm ngược lại do gây nguy hiểm.
Câu 6 :
a) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$b) n_{Al_2(SO_4)_3} = \dfrac{1}{2}n_{Al} = 0,1(mol)$
$m_{Al_2(SO_4)_3} = 0,1.342 = 34,2(gam)$
c)$n_{H_2SO_4} = \dfrac{3}{2}n_{Al} = 0,3(mol)$
$1600\ ml = 1,6\ lít$
$C_{M_{H_2SO_4}} = \dfrac{0,3}{1,6} = 0,1875M$
d) $n_{H_2} = n_{H_2SO_4} = 0,3(mol)$
$V_{H_2} = 0,3.22,4 = 6,72(lít)$
Câu 5: Bn có thể vào xem SGK lớp 9 nhé
Câu 6:
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
a. PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
b. Theo PT: \(n_{H_2SO_4}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\)
Đổi 1600ml = 1,6 lít
=> \(C_{M_{H_2SO_4}}=\dfrac{0,3}{1,6}=0,1875M\)
c. Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,3\left(mol\right)\)
=> \(V_{H_2}=0,3.22,4=6,72\left(lít\right)\)

câu 1,
PTHH: Fe3O4 + 4H2SO4--> FeSO4 + Fe2(SO4)3 + 4H2O
Na2O + H2SO4--> Na2SO4 + H2O
2Al(OH)3 +2 H2SO4--> Al2(SO4)3 + 2H2O
Zn + H2SO4-->ZnSO4 + H2
CaO + H2So4--> CaSO4 + H2O
câu 3: A
câu 1 :
Fe3O4 + 4H2SO4 -> FeSO4 + Fe2(SO4)3 +4 H2O
Na2O + H2SO4 -> Na2SO4\(\downarrow\) + H2O
2NaCl + H2SO4 -> Na2SO4\(\downarrow\) + HCl
2Al(OH)3 + 3H2SO4 -> Al2(SO4)3 + 6H2O
Zn + H2SO4 -> ZnSO4 + H2\(\)\(\uparrow\)
CaO + H2SO4 -> CaSO4 + H2O
A
A