Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ ZnO+2HCl\to ZnCl_2+H_2O\\ b,n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow n_{Zn}=0,15(mol)\Rightarrow m_{Zn}=0,15.65=9,75(g)\\ \Rightarrow \%_{Zn}=\dfrac{9,75}{25,95}.100\%=37,57\%\\ \Rightarrow \%_{ZnO}=(100-37,57)\%=62,43\%\\ c,n_{ZnO}=\dfrac{25,95-9,75}{81}=0,2(mol)\\ \Rightarrow n_{HCl}=2.0,15+2.0,2=0,7(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{0,7.36,5}{12\%}=212,92(g)\)

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
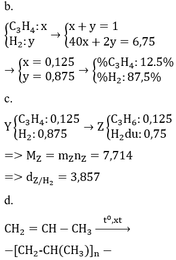


Thể tích khí đã tác dụng với dung dịch brom là : 6,72 - 2,24 = 4,48 (lít).
=> Số mol khí phản ứng với dung dịch brom là : 4,48/22,4 = 0,2 mol
Khối lượng bình brom tăng lên là do khối lượng hiđrocacbon bị hấp thụ. Vậy khối lượng mol phân tử của hiđrocacbon là :
5,6/0,2 = 28 (gam/mol)
=> Công thức phân tử của một hiđrocacbon là C 2 H 4
Dựa vào phản ứng đốt cháy tìm được hiđrocacbon còn lại là CH 4
% V C 2 H 4 = 4,48/6,72 x 100% = 66,67%; V CH 4 = 33,33%

Cho hỗn hợp qua dung dịch brom dư
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra là \(CH_4\)
\(CH_4+2O_2\rightarrow^{t^o}CO_2+2H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Ta có:
\(n_{CaCO_3}=\frac{40}{100}=0,4mol=n_{CO_2}=n_{CH_4}\)
\(\rightarrow V_{CH_4}=0,4.22,4=8,96l\)
\(\rightarrow\%V_{CH_4}=\frac{8,96}{13,56}=66\%\rightarrow\%V_{C_2H_4}=34\%\)

\(n_{P_2O_5}=\dfrac{28,4}{142}=0,2\left(mol\right)\)
\(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,4<--------------0,2
S + O2 --to--> SO2
0,25<----------0,25
=> \(\left\{{}\begin{matrix}\%m_P=\dfrac{0,4.31}{0,4.31+0,25.32}.100\%=60,78\%\\\%m_S=\dfrac{0,25.32}{0,4.31+0,25.32}.100\%=39,22\%\end{matrix}\right.\)

n Br2=\(\dfrac{32}{160}\)=0,2 mol
C2H2+2Br2->C2H2Br4
0,1------0,2 mol
=>%VC2H2=\(\dfrac{0,1.22,4}{5,6}\).100=40%
=>%VCH4=100-40=60%
=>n CH4=\(\dfrac{5,6-0,1.22,4}{22,4}\)=0,15 mol
CH4+2O2-to>CO2+2H2O
0,15----0,3
C2H2+\(\dfrac{5}{2}\)O2-to>2CO2+H2O
0,1-----0,25 mol
=>VO2=(0,3+0,25).22,4=12,32l

a) \(n_{Br_2\left(p\text{ư}\right)}=\dfrac{6,4}{160}=0,04\left(mol\right);n_{hh}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,04<--0,04
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,04}{0,6}.100\%=6,67\%\\\%V_{CH_4}=100\%-6,67\%=93,33\%\end{matrix}\right.\)
b) \(n_{CH_4}=0,6-0,04=0,56\left(mol\right)\)
PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
0,56----------->0,56
\(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
0,04----------->0,08
\(\Rightarrow V_{CO_2}=\left(0,08+0,56\right).22,4=14,336\left(l\right)\)
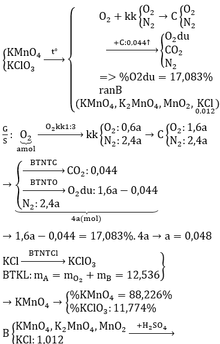
hỗn hợp X gồm gì thế em
Dạ em xin lỗi gồm C3H6 và C3H8