Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(m_{HCl}=\dfrac{150\cdot14,6\%}{100\%}=21,9g\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,6 0 0
0,2 0,4 0,2 0,2
0 0,2 0,2 0,2
Sau phản ứng, \(ddHCl\) còn dư và dư 0,2mol.
\(V_{H_2}=0,2\cdot22,4=4,48l\)

Bài 9:
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{14,6\%.100}{36,5}=0,4\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{0,4}{2}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,4-2.0,1=0,2\left(mol\right)\\ m_{HCl\left(dư\right)}=0,2.36,5=7,3\left(g\right)\)

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

Số mol của kẽm
nZn = \(\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,3 0,4 0,2 0,2
a) Lập tỉ số só sánh : \(\dfrac{0,3}{1}>\dfrac{0,4}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
Số mol dư của kẽm
ndư = nban đầu - nmol
= 0,3 - (\(\dfrac{0,4.1}{2}\))
= 0,1 (mol)
Khối lượng dư của kẽm
mdư = ndư . MZn
= 0,1 . 65
= 6,5 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mznCl2 = nZnCl2 . MZnCl2
= 0,2. 136
= 27,2 (g)
c) 4H2 + Fe3O4 → (to) 3Fe + 4H2O\(|\)
4 1 3 4
0,2 0,15
Số mol của sắt
nFe = \(\dfrac{0,2.3}{4}=0,15\left(mol\right)\)
Khối lượng của sắt
mFe = nFe. MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

Thiếu đề, anh cho là 100ml ddHCl 1M nhé
a,\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right);n_{HCl}=0,1.1=0,1\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,1 0,05 0,05
b,Ta có: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\) ⇒ Zn dư, HCl pứ hết
c,\(m_{ZnCl_2}=0,05.136=6,8\left(g\right)\)
\(V_{H_2}=0,05.22,4=1,12\left(l\right)\)

\(n_{Fe_2O_3}=\dfrac{3.2}{160}=0.02\left(mol\right)\)
\(n_{HCl}=\dfrac{2.19}{36.5}=0.06\left(mol\right)\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(1...........6\)
\(0.02...........0.06\)
Lập tỉ lệ : \(\dfrac{0.02}{1}>\dfrac{0.06}{6}\Rightarrow Fe_2O_3dư\)
\(n_{Fe_2O_3\left(dư\right)}=0.02-\dfrac{0.06}{6}=0.01\left(mol\right)\)
\(m_{Fe_2O_3\left(dư\right)}=0.01\cdot160=1.6\left(g\right)\)
\(m_{FeCl_3}=0.02\cdot162.5=3.25\left(g\right)\)
\(m_{H_2O}=0.03\cdot18=0.54\left(g\right)\)

a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\)
Vậy \(Al\left(OH\right)_3\) dư.
\(m_{dư}=0,75.78-98.0,5=9,5\left(g\right)\)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
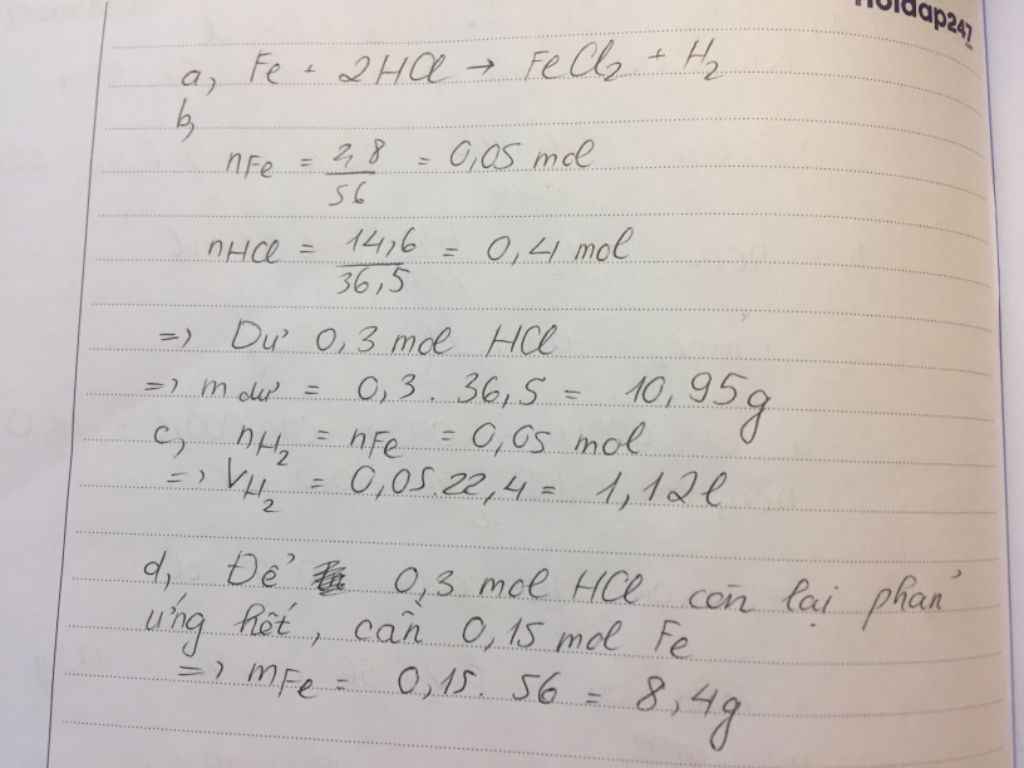
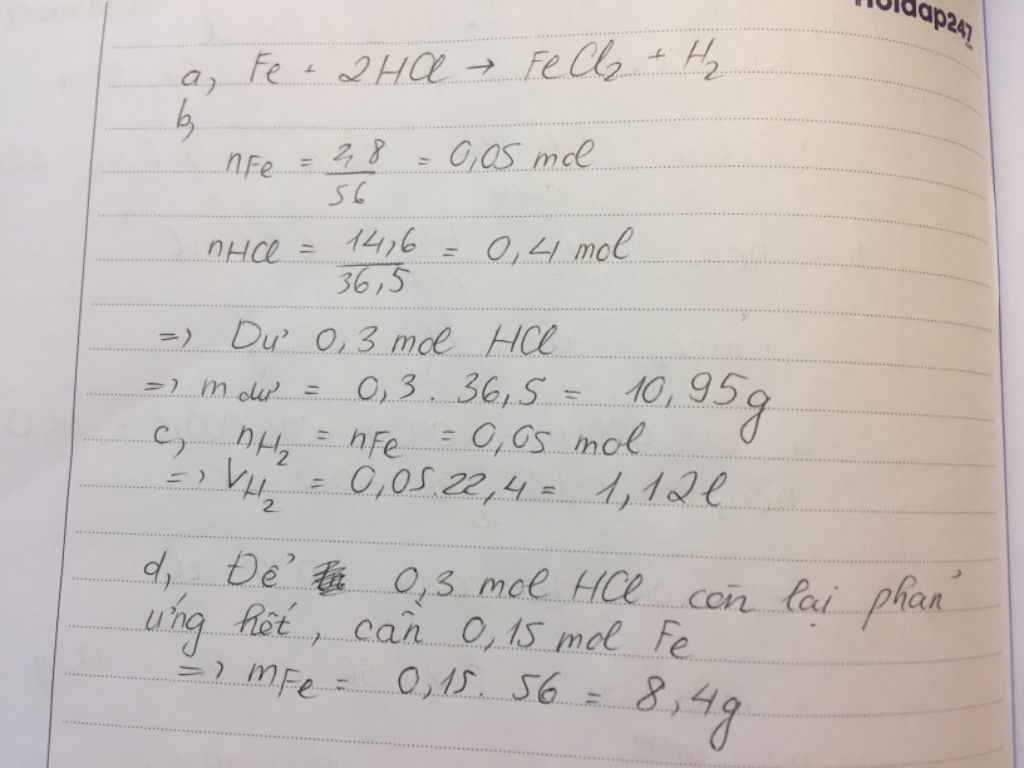

Ta có: \(n_{NaOH}=\dfrac{40.10\%}{40}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{100.14,6\%}{36,5}=0,4\left(mol\right)\)
a, PT: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,4}{1}\), ta được HCl dư.
Theo PT: \(n_{HCl\left(pư\right)}=n_{NaCl}=n_{NaOH}=0,1\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=0,4-0,1=0,3\left(mol\right)\)
\(\Rightarrow m_{HCl\left(dư\right)}=0,3.36,5=10,95\left(g\right)\)
b, \(C\%_{HCl}=\dfrac{10,95}{40+100}.100\%\approx7,82\%\)
\(C\%_{NaCl}=\dfrac{0,1.58,5}{40+100}.100\%\approx4,18\%\)