Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(m_{HCl}=\dfrac{200\cdot14,6\%}{100\%}=29,2g\Rightarrow n_{HCl}=0,8mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,8 0 0
0,1 0,2 0,1 0,1
0 0,6 0,1 0,1
b)Chất HCl dư và dư \(m=0,6\cdot36,5=21,9g\)
c)\(V_{H_2}=0,1\cdot22,4=2,24l\)
d)\(m_{H_2}=0,1\cdot2=0,2g\)
\(m_{ZnCl_2}=0,1\cdot136=13,6g\)
\(m_{ddZnCl_2}=6,5+200-0,2=206,3g\)
\(C\%=\dfrac{13,6}{206,3}\cdot100\%=6,59\%\)
a, ta có pt sau : Zn + 2HCl >ZnCl2 + H2 (1)
b, nHCl=\(\dfrac{200\times14,6}{100}=29,2\left(g\right)\)\(\Rightarrow n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
Ta có : nZn=\(\dfrac{6,5}{65}=0,1\left(mol\right)\)
Ta có tỉ lệ số mol là : \(\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,1}{1}< \dfrac{0,8}{2}\right)\)
\(\Rightarrow\) HCl dư , Zn pứ hết
Theo pt : nHClpứ = 2.nZn=2.0,1=0,2(mol)
\(\Rightarrow\)nHCl dư = nHCl bđ - nHCl pứ = 0,8 - 0,2 = 0,6 (mol)
\(\Rightarrow\)mHCl dư=0,6.36,6=21,9 (g)
c,theo pt :nH2=nZn=0,1(mol)
\(\Rightarrow\)VH2=0,1.22,4=2,24(l)
d,Các chất có trong dung dịch sau pứ là: ZnCl2 , HCl dư
mk chịu câu này ![]()

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

uiii em ơi, 2p mà viết và chụp xong luôn rồi à, nhanh thật, bái phục

\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{100\cdot14.6\%}{36.5}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1........2\)
\(0.1......0.4\)
\(LTL:\dfrac{0.1}{1}< \dfrac{0.4}{2}\Rightarrow HCldư\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=6.5+100-0.1\cdot2=106.3\left(g\right)\)
\(C\%ZnCl_2=\dfrac{0.1\cdot136}{106.3}\cdot100\%=12.79\%\)
\(C\%HCl\left(dư\right)=\dfrac{\left(0.4-0.2\right)\cdot36.5}{106.3}\cdot100\%=6.87\%\%\)

a. \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b. \(n_{Mg}=\dfrac{2.4}{24}=0.1mol\)
\(mct_{HCl}=\dfrac{500\times36.5}{100}=182.5g\Rightarrow n_{HCl}=\dfrac{182.5}{36.5}=5mol\)
Ta có: \(\dfrac{0.1}{1}< \dfrac{5}{2}\Rightarrow\) HCl dư
nHCl phản ứng = 0.2 mol => nHCl dư = 5 - 0.2 = 4.8 mol
mHCl dư = \(4.8\times36.5=175.2g\)
c. \(V_{H_2}=0.1\times22.4=2.24l\)
d. mdd sau phản ứng = \(2.4+500-0.1\times2=502.2g\)
\(C\%_{MgCl_2}=\dfrac{0.1\times95\times100}{502.2}=1.89\%\)

1.
a, \(n_{Mg}=\dfrac{3,6}{24}=0,15\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,15 0,3
b, Ta có: \(\dfrac{0,15}{1}< \dfrac{0,5}{2}\) ⇒ Mg pứ hết, HCl dư
\(m_{HCldư}=\left(0,5-0,3\right).36,5=7,3\left(g\right)\)
c, \(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
2.
a, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 ---to→ 2P2O5
Mol: 0,2 0,25 0,1
b, \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c, \(m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(V_{kk}=5,6.5=28\left(l\right)\)

\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 < 0,4 ( mol )
0,1 0,2 0,1 ( mol )
Chất dư là HCl
\(n_{HCl\left(dư\right)}=0,4-0,2=0,2mol\)
\(V_{H_2}=0,1.22,4=2,24l\)

Fe + 2HCl -> FeCl2 + H2
nFe = 5,6/56 = 0,1 mol
=>nH2 = 0,1 mol
=> VH2= 0,1*22,4= 2,24 lít
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,1-->0,2------------------>0,1
=> \(\left\{{}\begin{matrix}m_{ddHCl}=\dfrac{0,2.36,5}{15\%}=\dfrac{146}{3}\left(g\right)\\V_{H_2}=0,1.22,4=4,48\left(l\right)\end{matrix}\right.\)

\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{1+35,5}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
n(mol) 0,2------->0,4--------->0,2---->0,2
\(\dfrac{n_{Fe}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,2}{1}< \dfrac{0,5}{2}\right)\)
`=> Fe` hết, `HCl` dư, tính theo `Fe`
\(n_{HCl\left(dư\right)}=0,5-0,4=0,1\left(mol\right)\\ m_{HCl\left(dư\right)}=n\cdot M=0,1\cdot\left(1+35,5\right)=3,65\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,2\cdot22,4=4,48\left(l\right)\)
a) Ta có : PTHH : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có : \(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
Theo PTHH thì ta có : \(2n_{Fe}=n_{HCl}\)
Giả sử HCl dùng hết : \(\Rightarrow n_{Fe}\) cần dùng là : \(0,25\left(mol\right)\) không thỏa mãn
\(\Rightarrow Fe\) dùng hết ; HCl dư
Số mol HCl dư là :
\(0,5-0,2.2=0,1\left(mol\right)\)
Khối lượng dư của HCl là :
\(0,1.36,5=3,65\left(g\right)\)
b) Do Fe dùng hết nên ta tính H theo Fe
Theo PTHH : \(n_{Fe}=n_{H_2}\)
\(\Rightarrow n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
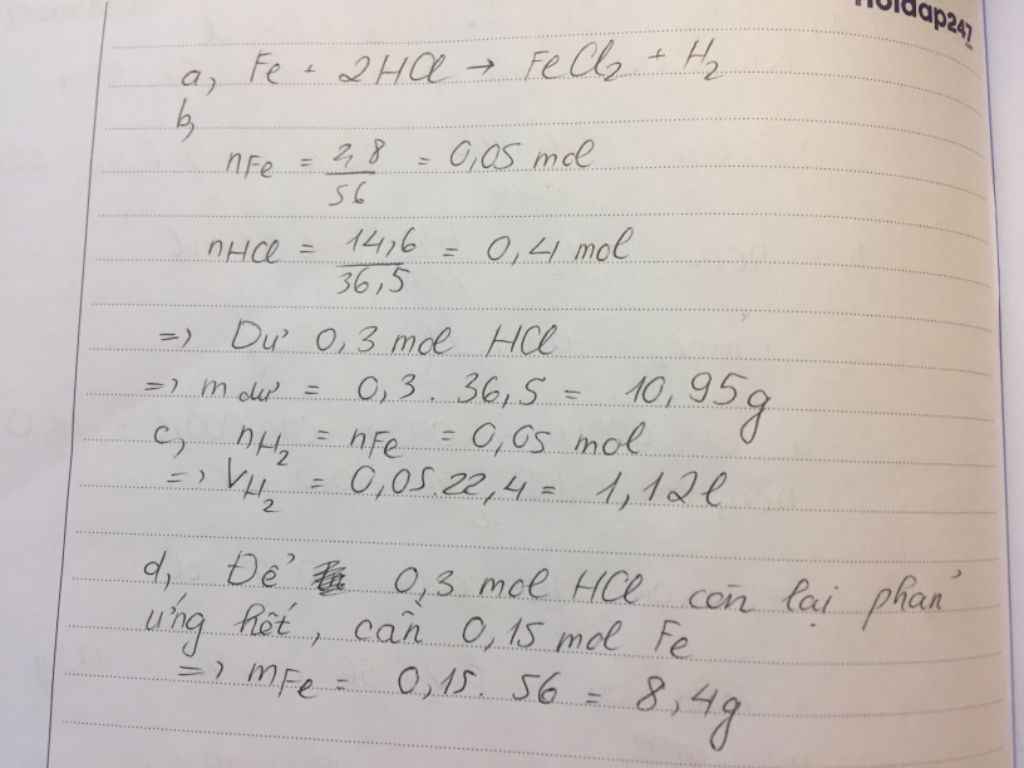
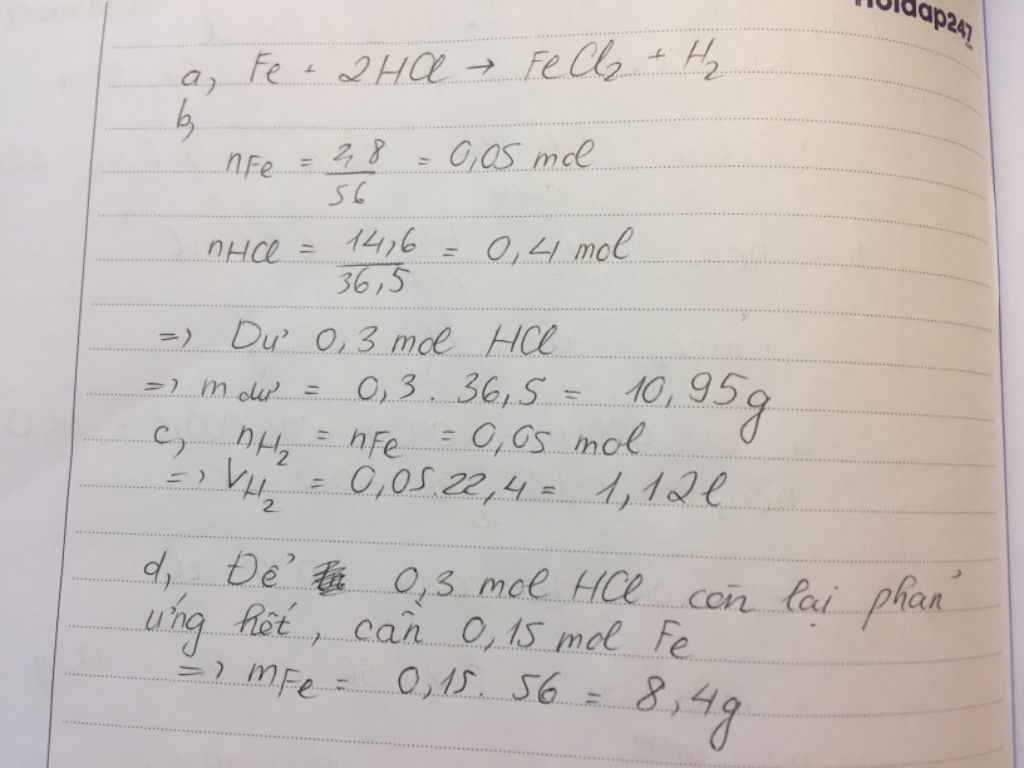
\(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(m_{HCl}=\dfrac{150\cdot14,6\%}{100\%}=21,9g\Rightarrow n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,6 0 0
0,2 0,4 0,2 0,2
0 0,2 0,2 0,2
Sau phản ứng, \(ddHCl\) còn dư và dư 0,2mol.
\(V_{H_2}=0,2\cdot22,4=4,48l\)