Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\left[OH^-\right]=0,001M\\ \Rightarrow pH=14-pOH=14+log\left[OH^-\right]=14+log\left[0,001\right]=14-3=11\)

[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
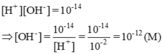
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ

Câu 3 :
\(pH=-log\left[H^+\right]=-log\left(0.1\right)=1\)
Câu 4 :
Chứa các ion : H+ , Cl-
Câu 5 :
\(n_{NaOH}=n_{HCl}=0.02\cdot0.1=0.002\left(mol\right)\)
\(\Rightarrow x=\dfrac{0.002}{0.01}=0.2\left(M\right)\)
Câu 1 :
Bảo toàn điện tích :
\(n_{SO_4^{2-}}=\dfrac{0.2\cdot2+0.1-0.05}{2}=0.225\left(mol\right)\)
\(m_{Muối}=0.2\cdot64+0.1\cdot39+0.05\cdot35.5+0.225\cdot96=40.075\left(g\right)\)
Câu 2 :
\(\left[Na^+\right]=\dfrac{0.15\cdot0.5\cdot2+0.05\cdot1}{0.15+0.05}=1\left(M\right)\)

Dung dịch axit ban đầu có [H+] = 0,1 M
⇒ nH+= 0,1.0,1 = 0,01 mol
Dung dịch sau phản ứng có pH = 12
⇒ dư bazơ và có pOH =14 – 12 = 2
⇒ [OH-] = 0,01M
⇒ nOH− dư = 0,002 mol
Phản ứng trung hòa:
nH+phản ứng = nOH−phản ứng = 0,01 mol
⇒ nNaOH ban đầu = nOH−phản ứng + nOH− dư
= 0,01 + 0,002 = 0,012 mol
⇒ a = 0,12M

Đáp án A
pH = 11 => OH- dư sau phản ứng => pOH =3
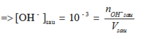
=> nOH- sau = Vsau . [OH-] = 10-3. 0,6= 0,0006 = 6.10-4 (mol)
pH = 2 => [H+]= 10-2 = 0,01M => nH+= 0,3 . 0,01= 0,003
nOH- = 0,3.a
H+ + OH- → H2O
Ban đầu: 0,003 0,3.a
Phản ứng: 0,003 0,003
Sau: 0 0,3.a-0,003
nOH- sau= 6.10-4 = 0,3a -0,003 => a=0,012M

Đáp án D
Có [H+]H2SO4>[H+]HCl>[H+]NH4Cl>[H+]NaOH nên b < a< c < d

Chọn đáp án D
Đây là 2 dung dịch có môi trường bazo.NaOH có tính bazo mạnh hơn nên x >y.

\(3.\\ a.\left[H^+\right]=\dfrac{10^{-14}}{\left[OH^-\right]}=\dfrac{10^{-14}}{10^{-5,17}}=10^{-8,83}\left(mol\cdot L^{-1}\right)\\ pH=-log\left[H^+\right]=8,83\)
b. pH > 7: dầu gội có môi trường base
4.
a. pH < 7 nên đó là môi trường acid.
b.
+ Tưới tiêu nước rửa chua.
+ Dùng vôi bột bón cho đất để trung hoà, giảm chua.
+ Bón phân hữu cơ, phân chuồng,...
5.
\(A.pH=-log\left(0,1\right)=1\\ B.pH>1\\ C.pH=7\\ D.pH=-log\left(\dfrac{10^{-14}}{0,01}\right)=12\)
Vậy chọn D.