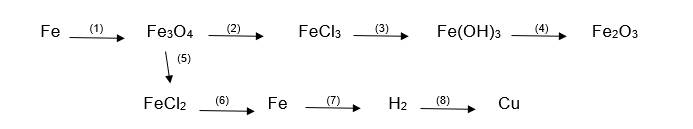
Viết phương trình hóa học biểu diễn chuyển đổi hóa học sau:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


(1) \(3Fe+2O_2\xrightarrow[]{t^\circ}Fe_3O_4\)
(2) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(3) \(FeCl_3+3LiOH\xrightarrow[]{}Fe\left(OH\right)_3\downarrow+3LiCl\)
(4) \(2Fe\left(OH\right)_3\xrightarrow[]{t^\circ}Fe_2O_3+3H_2O\)
(5) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(6) \(FeCl_2\xrightarrow[]{đpdd}Fe+Cl_2\uparrow\)
(7) \(Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\uparrow\)
(8) \(H_2+CuO\xrightarrow[]{t^\circ}Cu+H_2O\uparrow\)

a) \(M_R=2M_O=2\cdot16=32\left(\text{g/mol}\right)\)
\(\Rightarrow\) R là nguyên tố lưu huỳnh (S).
b) Số p = số e = 16 (hạt).

Cho các chất sau: (1) Khí nitơ do nguyên tố N tạo nên;(2) Khí cacbonic do 2 nguyên tố C và O tạo nên;(3) Natri hiđroxit do 3 nguyên tố Na, O và H tạo nên;(4) Lưu huỳnh do nguyên tố S tạo nên.Trong những chất trên, chất nào là đơn chất
A. (1); (2).
B. (2); (3).
C. (3); (4).
D. (1); (4).

1 lít khí có số mol khí là \(\dfrac{1,45}{29}=0,05\left(mol\right)\)
=> 1,5 lít khí có số mol là \(\dfrac{1,5}{1}.0,05=0,075\left(mol\right)\)
Vậy số mol của CO2 là 0,075 mol
(1) \(3Fe+2O_2\xrightarrow[]{t^\circ}Fe_3O_4\)
(2) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(3) \(FeCl_3+3LiOH\xrightarrow[]{}Fe\left(OH\right)_3\downarrow+3LiCl\)
(4) \(2Fe\left(OH\right)_3\xrightarrow[]{t^\circ}Fe_2O_3+3H_2O\)
(5) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(6) \(FeCl_2\xrightarrow[]{đpdd}Fe+Cl_2\uparrow\)
(7) \(Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\uparrow\)
(8) \(H_2+CuO\xrightarrow[]{t^\circ}Cu+H_2O\uparrow\)
(1) 3��+2�2→�∘��3�43Fe+2O2t∘Fe3O4
(2) ��3�4+8���→����2+2����3+4�2�Fe3O4+8HClFeCl2+2FeCl3+4H2O
(3) ����3+3����→��(��)3↓+3����FeCl3+3LiOHFe(OH)3↓+3LiCl
(4) 2��(��)3→�∘��2�3+3�2�2Fe(OH)3t∘Fe2O3+3H2O
(5) ��3�4+8���→����2+2����3+4�2�Fe3O4+8HClFeCl2+2FeCl3+4H2O
(6) ����2→đ�����+��2↑FeCl2đpddFe+Cl2↑
(7) ��+2���→����2+�2↑Fe+2HClFeCl2+H2↑
(8) �2+���→�∘��+�2�↑H2+CuOt∘Cu+H2O↑