Cho 1,44g một kim loại R có hoá trị II phản ứng hoàn toàn trong 250ml dung dịch H2SO4 0,3M. Dung dịch thu được còn chứa axit dư và phải trung hoà axit dư bằng 60ml dung dịch NaOH 0,5M. Hãy xác định kim loại R
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


R+H2SO4->R2(SO4)n+H2(1)
H2SO4+2NaOH->Na2SO4+2H2O(2)
nNaOH=0,06.0,5=0,03(mol)
->nH2SO4 dư sau phản ứng (1)=0,03/2=0,015(mol)
Mà nH2SO4 ban đầu =0,25.0,3=0.075 mol
->nH2SO4 cần cho phản ứng (1) =0,075-0,015=0,06(mol)
->nR=nH2SO4=0,06
->MR=1,44/0,06=24(Mg)

Đổi 250 ml= 0,25 l ; 60ml = 0,06 l
Gọi kim loại cần tìm là M, số mol M là a (mol)
Số mol H2SO4 là: 0,25 x 0,3 = 0,075 (mol)
Số mol NaOH là: 0,06 x 0,5= 0,03 (mol)
M + H2SO4 = MSO4 + H2
a a (mol)
2NaOH + H2SO4 = Na2SO4 + 2H2O
(0,15-2a) (0,075-a) (mol)
Vì số mol H2SO4 dư tác dụng vừa đủ với số mol NaOH
=> 0,15 - 2a = 0,03 (mol)
=> a= 0,06 (mol)
Khối lượng mol của kim loại M là:
1,44: 0,06= 24 (g)
Vậy M là kim loại Mg

Đáp án C
nH+ pứ KL = 2nH2SO4 – nNaOH = 0,12 mol = 2nKL
=> nKL = 0,06 mol => MKL = 24g (Mg)

Số mol H 2 S O 4 trong 100ml dung dịch 0,5M là :
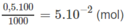
Số mol NaOH trong 33,4 ml nồng độ 1M :
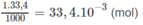
H 2 S O 4 + 2NaOH → N a 2 S O 4 + 2 H 2 O
Lượng H 2 S O 4 đã phản ứng với NaOH :

Số mol H 2 S O 4 đã phản ứng với kim loại là :
5. 10 - 2 - 1.67. 10 - 2 = 3,33. 10 - 2 mol
Dung dịch H 2 S O 4 0,5M là dung dịch loãng nên :
X + H 2 S O 4 → X S O 4 + H 2 ↑
Số mol X và số mol H 2 S O 4 phản ứng bằng nhau, nên :
3,33. 10 - 2 mol X có khối lượng 0,8 g
1 mol X có khối lượng: 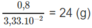
⇒ Mkim loại = 24 g/mol.
Vậy kim loại hoá trị II là magie.

a) nH2SO4= 0,25 . 0,3 = 0,075 ( mol )
nNaOH = 0,06 . 0,5 = 0,03 ( mol )
2NaOH + H2SO4 \(\rightarrow\) Na2SO4 + 2H2O
0,03______0,015_____0,015___0,03 ( mol )
nH2SO4 ( tham gia phản ứng với kim loại ) = 0,075 - 0,015 = 0,06 (mol)
Gọi A là kim loại hoá trị II
A + H2SO4 \(\rightarrow\) ASO4 + H2
0,06__0,06____0,06___0,06 (mol)
MA = \(\dfrac{1,44}{0,06}\)= 24 ( g/mol)
Vậy A là Magie . CTHH : Mg
b) nHCl = 0,3 . 0,5 = 0,15 (mol)
nBa(OH)2 = 0,2 . a = 0,2a ( mol)
Do HCl dư nên ta sẽ kê số mol của Ba(OH)2 vào phương trình
2HCl + Ba(OH)2 \(\rightarrow\) BaCl2 + 2H2O
0,4a____0,2a_______0,2a___0,4a ( mol )
nHCl dư = 0,15 - 0,4a
CM HCl dư = \(\dfrac{0,15-0,4a}{0,5}\) = 0,02
=> 0,15 - 0,4a = 0,01
=> a = \(\dfrac{0,15-0,01}{0,4}\)= 0,35 (M)

Gọi kim loại cần tìm là R
\(n_{H_2SO_4}=0,25.0,3=0,075\left(mol\right)\)
\(n_{KOH}=0,06.0,5=0,03\left(mol\right)\)
PTHH: R + H2SO4 --> RSO4 + H2
0,06<--0,06
2KOH + H2SO4 --> K2SO4 + 2H2O
0,03-->0,015
=> \(M_R=\dfrac{1,44}{0,06}=24\left(g/mol\right)\)
=> R là Mg
Số mol H2SO4 và KOH lần lượt là 0,3.0,25=0,075 (mol) và 0,5.0,06=0,03 (mol).
Số mol H2SO4 phản ứng là (0,075.2-0,03):2=0,06 (mol) và bằng số mol của kim loại ban đầu.
Nguyên tử khối của kim loại cần tìm là 1,44:0,06=24 (g/mol).
Vậy kim loại đã cho là magie (Mg).

Gọi kim loại là M
M + H2SO4 ---> MSO4 + H2 (1)
H2SO4 + 2NaOH ---> Na2SO4 + 2H2O (2)
Số mol H2SO4 ban đầu = 0,5.0,15 = 0,075 mol; số mol H2SO4 dư = 1/2 số mol NaOH = 0,5.1.0,03 = 0,015 mol. Số mol H2SO4 phản ứng (1) = 0,075 - 0,015 = 0,06.
số mol muối MSO4 = số mol H2SO4 p.ư (1) nên: M + 96 = 7,2/0,06 = 120. Vậy: M = 24 (Mg).

Sửa đề: Hòa tan hoàn toàn 1,44 kim loại hóa trị II.......
Đổi 250ml = 0,25l; 60ml = 0,06l
\(n_{H_2SO_4}=0,25.0,3=0,075\left(mol\right)\)
\(n_{NaOH}=0,06.0,5=0,03\left(mol\right)\)
PTHH: \(2NaOH+H_2SO_4->Na_2SO_4+2H_2O\left(1\right)\)
Theo PT ta có tỉ lập tỉ lệ:
\(\dfrac{0,075}{2}>\dfrac{0,03}{1}\Rightarrow\) \(H_2SO_4\) dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=\dfrac{0,03.1}{2}=0,015\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,075-0,015=0,06\left(mol\right)\)
- \(X+H_2SO_4\rightarrow XSO_4+H_2\left(2\right)\)
Theo PT (2) ta có: \(n_X=n_{H_2SO_4}=0,06\left(mol\right)\)
\(\Rightarrow M_X=\dfrac{1,44}{0,06}=24\left(g/mol\right)\)
Vậy X là kim loại Magie (Mg)
\(n_{NaOH}=0.06\cdot0.5=0.03\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\dfrac{0.03}{2}=0.015\left(mol\right)\)
\(n_{H_2SO_4\left(pư\right)}=0.25\cdot0.3-0.015=0.06\left(mol\right)\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(0.06....0.06\)
\(M_R=\dfrac{1.44}{0.06}=24\left(\dfrac{g}{mol}\right)\)
\(R:Mg\)
n NaOH = 0,06.0,5 = 0,03(mol)
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
n H2SO4 dư = 1/2 n NaOH = 0,015(mol)
n H2SO4 pư = 0,25.0,3 - 0,015 = 0,06(mol)
$R + H_2SO_4 \to RSO_4 + H_2$
n R = n H2SO4 pư = 0,06(mol)
M R = 1,44/0,06 = 24(Mg)
Vậy R là Magie