Phân tử 1 hợp chất gồm 2 nguyên tử nguyên tố x liên kết với một nguyên tử hidro và nặng gấp 9 lần phần tử H2. Tìm công thức x . Tính phần trăm mỗi nguyên tố trong hợp chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)Gọi hợp chất cần tìm là \(X_2O_3\)
Theo bài ta có: \(PTK_{X_2O_3}=76M_{H_2}=76\cdot2=152\left(đvC\right)\)
b)Mà \(2M_X+3M_O=152\Rightarrow M_X=\dfrac{152-3\cdot16}{2}=52\left(đvC\right)\)
X là nguyên tố Crom(Cr).
Vậy CTHH là \(Cr_2O_3\).
c)\(\%X=\dfrac{2\cdot52}{2\cdot52+3\cdot16}\cdot100\%=68,42\%\)

Gọi công thức hóa học A : XH4
Vì phân tử chất đó nặng gấp 8 lần phân tử Hiđrô nên :
\(\frac{M_A}{2.M_H}=8\)
\(\frac{M_A}{2.1}=8\)
\(\rightarrow M_A=16\)
Mặt khác :
\(M_A=M_X+4.M_H\)
\(\rightarrow M_X+4=16\)
\(M_X=12\)
\(\rightarrow X\) là Cacbon, ký hiệu là C, nguyên tử khối là 12 đvC.
\(\%X=\frac{M_X}{M_A}.100\%=\frac{12}{16}.100\%=75\%\)
Vậy ...
Ta có :
PTKH = 1 * 2 = 2 đvC
=> PTKhợp chất = 2 * 8 = 16 đvC
do hợp chất gồm nguyên tử nguyên tố X và 4 nguyên tử Hiđro
=> PTKhợp chất = NTKX + NTKH * 4
=> 16 đvC = NTKX + 4 đvC
=> NTKX = 12 đvC
=> X là nguyên tố Cacbon (C)
=> % của X trong hợp chất trên là :
12 : 16 * 100% = 75%

Câu 5 :
$PTK = 1X + 3H = 1X + 3.1 = 8,5M_{H_2} = 8,5.2 = 17(đvC)$
$\Rightarrow X = 14(đvC)$ - Suy ra X là Nito
Vậy CTHH của hợp chất là $NH_3$(khí amoniac)
Câu 6 :
$PTK = 1Y + 3O = 1Y + 3.16 = 5M_O = 5.16 = 80$
$\Rightarrow Y = 32(đvC)$ - Suy ra Y là Lưu huỳnh
Vậy CTHH của hợp chất là $SO_3$
Câu 5:
Gọi CTHH là: XH3
Theo đề, ta có: \(d_{\dfrac{XH_3}{H_2}}=\dfrac{M_{XH_3}}{M_{H_2}}=\dfrac{M_{XH_3}}{2}=8,5\left(lần\right)\)
=> \(M_{XH_3}=17\left(g\right)\)
Ta có: \(M_{XH_3}=NTK_X+1.3=17\left(g\right)\)
=> NTKX = 14(đvC)
=> X là nitơ (N)
Vậy CTHH là NH3
Câu 6:
Gọi CTHH của hợp chất A là: YO3
Theo đề, ta có:
\(d_{\dfrac{YO_3}{O}}=\dfrac{M_{YO_3}}{M_O}=\dfrac{M_{YO_3}}{16}=5\left(lần\right)\)
=> \(M_{YO_3}=80\left(g\right)\)
Ta có: \(M_{YO_3}=NTK_Y+16.3=80\left(g\right)\)
=> NYKY = 32(đvC)
=> Y là lưu huỳnh (S)
Vậy CTHH của A là SO3

a) Công thức tồng quát của hợp chất A : K2X
b) Ta có : MA=47MH2
=> MA=47.2=94
c) Ta có : 39.2 + X=94
=> X= 16
=> X là Oxi (O)

1.
a) NTK của O = 16
=> PTK của hợp chất = 16
Lại có phân tử gồm 1 nguyên tử x và 4 nguyên tử H
=> PTK của hợp chất = 1x + 4H = 16
<=> x + 4.1 = 16
<=> x + 4 = 16
<=> x = 12
=> x là Cacbon ( C )
b) Phần trăm theo khối lượng của nguyên tố x trong hợp chất = \(\frac{12}{16}\cdot100=75\%\)
2.
Phân tử của hợp chất gồm 2 nguyên tử nguyên tố x liên kết với 1 nguyên tố O
Lại có PTK của hợp chất = 62
=> PTK của hợp chất = 2x + 1O = 62
<=> 2x + 1.16 = 62
<=> 2x + 16 = 62
<=> 2x = 46
<=> x = 23
=> x là Natri ( Na )

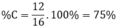
\(CT:X_2H\)
\(M_A=2\cdot9=18\left(\text{g/mol}\right)\)
\(\Leftrightarrow2X+1=18\)
\(\Leftrightarrow X=8.5\)
=> Đề sai
Sửa đề : 1 hợp chất gồm 2 nguyên từ H liên kết với một nguyên tử hidro
CTHH hợp chất : H2X
M H2X = 2 + X = 9.2 = 18
=> X = 16(Oxi)
Vậy hợp chất là H2O
%H = 2/18 .100% = 11,11%
%O = 100% -11,11% = 88,89%