nguyên tử của nguyên tố x có tổng số hạt nhân là 40. số hạt mang điện nhiều hơn hạt không mang điện là 12. xác định vị trí của nguyên tố x trong bảng tuần hoàn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố A là 58 : p + e + n = 58 hay 2p + n = 58 (do p = e) (1)
Số hạt p ít hơn số hạt n là 1 hạt : n - p =1 (2)
Giải (1), (2) ta có p = e = 19, n = 20
Vậy số hiệu nguyên tử (z) = 19
Số khối (A) = p + n = 19 + 20 = 39
Kí hiệu nguyên tử:

gọi số prton,electron và notron của X lần lượt là :p,e,n
do p=e=> p+e=2p
theo đề ta có hpt: \(\begin{cases}2p+n=52\\2p=1,889n\end{cases}\)
<=> \(\begin{cases}p=17\\n=18\end{cases}\)
do p=17
=> x là Clo (Cl)
Cl nằm ở ô thứ 17 trong BTH

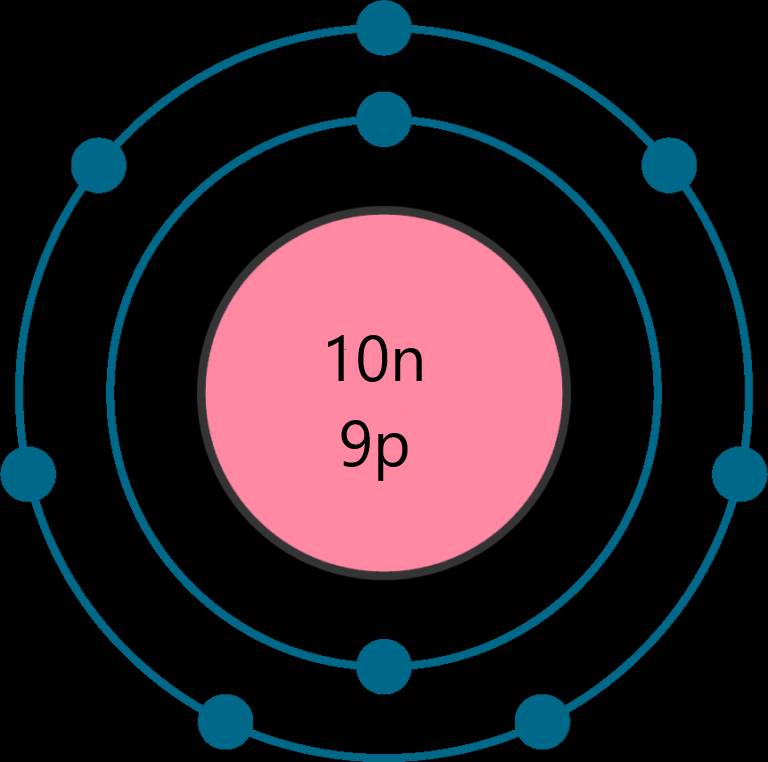
Tổng số các loại hạt là 28, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8
⇒ Số neutron là 10 hạt
Số proton là 9 hạt
Số electron là 9 hạt
⇒ Nguyên tố Fluorine - ô số 9, chu kì 2, nhóm VIIA trong bảng tuần hoàn

1) a) \(Tacó:\left\{{}\begin{matrix}2Z+N=40\\2Z-N=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}Z=13\\N=14\end{matrix}\right.\\ \Rightarrow A=Z+N=13+14=27\)
b) Z=13 => X là Nhôm (Al)
c) Cấu hình e: \(1s^22s^22p^63s^23p^1\)
X thuộc ô 13, chu kỳ 3, nhóm IIIA
d) \(4Al+3O_2-^{t^o}\rightarrow2Al_2O_3\\Al+\dfrac{3}{2}Cl_2 -^{t^o}\rightarrow AlCl_3\\ 2Al+3S-^{t^o}\rightarrow Al_2S_3\\ Al+3HCl\rightarrow AlCl_3+\dfrac{3}{2}H_2\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
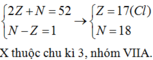


Số hạt mang điện là:(40 + 12): 2 = 26 hạt
Số hạt không mang điện là: 40 - 26 = 14 hạt
Nguyên tố x là Fe(sắt) vì trong bảng tuần hoàn hoá học điện tích hạt nhân của Fe = 26.