Đốt cháy hỗn hợp gồm một số hiđrocacbon cần V lít O2 (đktc), thu được 2,24 lít CO2 (đktc) và 2,7 gam H2O. Giá trị của V là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
Bảo toàn O : 2nO2 = 2nCO2 + nH2O
=> nO2 = 0,175 mol
=>V= 3,92 lit

Ta có nCO2 = 0,1 mol, nH2O = 0,15 mol, bảo toàn O => VO2 = 3,92 lít
=> Đáp án D

Chọn đáp án B
Đốt hỗn hợp các ankan ta luôn có: nCO2 – nH2O = nHỗn hợp ankan
nCO2 = nH2O – nHỗn hợp ankan = 0,4 – 0,1 = 0,3 mol.
⇒ VCO2 = 6,72 lít

Chọn đáp án B
Đốt hỗn hợp các ankan ta luôn có: nCO2 – nH2O = nHỗn hợp ankan
nCO2 = nH2O – nHỗn hợp ankan = 0,4 – 0,1 = 0,3 mol.
⇒ VCO2 = 6,72 lít ⇒ Chọn B

Đáp án A
nX = 0,1 mol; nH2O = 0,35 mol
nX = nH2O - nCO2 => nCO2 = 0,35 - 0,1 = 0,25 mol
→ V = 22,4.0,25 = 5,6 lít

Chọn đáp án D
Vì n C O 2 = n H 2 O = 1 , 3 m o l ⇒ Cả 3 este đều có dạng CnH2nO2
BTTN (O) ⇒ n O 2 = 1 , 3 × 2 + 1 , 3 - 0 , 4 × 2 2 = 1 , 55 m o l
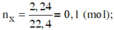
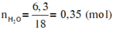
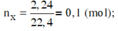
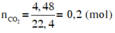
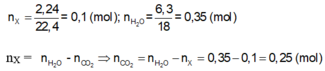
PTHH :
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2\uparrow+2H_2O\)
trc p/u : 0,1 0,15
p/u : 0,05 0,15 0,1 0,1
sau p/u: 0,05 0,15 0 0,05
-----> H2O dư
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\)
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
Ta có: \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\)
BTNT O, có: 2nO2 = 2nCO2 + nH2O
⇒ nO2 = 0,175 (mol)
\(\Rightarrow V_{O_2}=0,175.22,4=3,92\left(l\right)\)