Cho m gam hỗn hợp Fe và FeS hòa tan vào dung dịch HCl dư thu được hỗn hợp khí.
Dẫn hỗn hợp này qua dung dịch Cu(NO3)2 dư thu được 9,6 gam kết tủa đen và có 4,48 lít khí
(đktc) thoát ra. Giá trị của m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$a\big)$
$Zn+2HCl\to ZnCl_2+H_2$
$ZnS+2HCl\to ZnCl_2+H_2S$
$b\big)$
Đặt $n_{Zn}=x(mol);n_{ZnS}=y(mol)$
$\to 65x+97y=16,2(1)$
Theo PT: $n_{H_2}=x;n_{H_2S}=y$
$\to x+y=\frac{4,48}{22,4}=0,2(2)$
Từ $(1)(2)\to x=y=0,1(mol)$
$Cu(NO_3)_2+H_2S\to CuS\downarrow+2HNO_3$
Theo PT: $n_{CuS}=n_{H_2S}=0,1(mol)$
$\to m=0,1.96=9,6(g)$

Đáp án B
Lời giải chi tiết
Có m(hh khí) = 6,11; n(hh khí) = 0,13
=> n(Cl2) = 0,05; n(O2) = 0,08.
Hòa tan hết Y trong HCl nên có: n(HCl) = 2.n(H2O) = 2.n(O2-) = 0,32 mol
- BTNT (Cl):
n(Cl- trong Z) = n(AgCl) = n(HCl) + n(Cl-) = 0,32 + 0,1 = 0,42. → m(AgCl) = 0,42.143,5 = 60,27 gam
→ m(kết tủa) = m(AgCl) + m(Ag) → m(Ag) = 73,23 – 60,27 = 12,96 → n(Ag) = 0,12 mol.
=> n(Fe2+) = 0,12.
BTĐT trong Z: 2.0,12 + 2.n(Cu) = 0,42 => n(Cu) = 0,09.
Vậy X chứa Fe (0,12) và Cu(0,09).
Khi X tác dụng HNO3, ta thấy: (0,12 × 3 + 0,09 × 2) ÷ 3 = 0,18 mol > n(NO) = 0,15 mol
có nghĩa là Fe không lên hết Fe3+ mà có 1 phần chỉ lên Fe2+
Khi phản ứng với HNO3: nFe(III) = a mol ; nFe(II) = bmol. ta có hệ:
a + b = 0,12
3a + 2b + 0,09.2 = 0,15.3
Giải hệ: a = 0,03; b = 0,09.
Vì HNO3 dùng hết, n(HNO3) = 4n(NO) = 0,6 mol → m(HNO3) = 37,8 → m(dd HNO3) = 120 gam.
→ BTKL: m(dd T) = m(X) + m(HNO3) – m(NO) = 127,98 gam.
C%(Fe(NO3)3 trong T) = 0,03 . 242 : 127,98 ≈ 5,67%.

Đáp án B
Có m h h k h í = 6,11; n h h k h í = 0,13
=> n C l 2 = 0,05; n O 2 = 0,08.
Hòa tan hết Y trong HCl nên có: n H C l = 2. n H 2 O = 2. n O 2 - = 0,32 mol
- BTNT (Cl):
n C l - t r o n g Z = n A g C l = n H C l + n C l - = 0,32 + 0,1 = 0,42. → m A g C l = 0,42.143,5 = 60,27 gam
→ m k ế t t ủ a = m A g C l + m A g → m A g = 73,23 – 60,27 = 12,96 → n A g = 0,12 mol.
=> n F e 2 + = 0,12.
BTĐT trong Z: 2.0,12 + 2. n C u = 0,42 => n C u = 0,09.
Vậy X chứa Fe (0,12) và Cu(0,09).
Khi X tác dụng HNO3, ta thấy: (0,12 × 3 + 0,09 × 2) ÷ 3 = 0,18 mol > n N O = 0,15 mol
có nghĩa là Fe không lên hết Fe3+ mà có 1 phần chỉ lên Fe2+
Khi phản ứng với HNO3: nFe(III) = a mol ; nFe(II) = bmol. ta có hệ:
a + b = 0,12
3a + 2b + 0,09.2 = 0,15.3
Giải hệ: a = 0,03; b = 0,09.
Vì HNO3 dùng hết, n H N O 3 = 4 n N O = 0,6 mol → m H N O 3 = 37,8 → m d d H N O 3 = 120 gam.
→ BTKL: m d d T = m X + m H N O 3 - m N O = 127,98 gam.
% C F e ( N O 3 ) 3 t r o n g T = 0,03 . 242 : 127,98 ≈ 5,67%.

Đáp án A
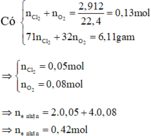
Y + HCl => Z chỉ chứa hai muối, HCl phản ứng hết
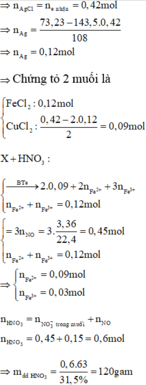
⇒ m dd T = 120 + 64 . 0 , 09 + 56 . 0 , 12 - 30 . 0 , 15 = 127 , 98 gam ⇒ C % Fe NO 3 3 = 242 . 0 , 03 127 , 98 . 100 % = 5 , 67 %
gần với giá trị 5% nhất

`Fe + 2HCl -> FeCl_2 + H_2 ↑`
`0,2` `0,2` `(mol)`
`FeS + 2HCl -> FeCl_2 + H_2 S↑`
`0,1` `0,1` `(mol)`
`H_2 S + Pb(NO_3)_2 -> PbS↓ + 2HNO_3`
`0,1` `0,1` `(mol)`
`n_[PbS] = [ 23,9 ] / 239 = 0,1 (mol)`
`n_Y = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
`a)` Hỗn hợp `Y` gồm khí `H_2` và `H_2 S`
`=> n_[H_2 S] = 0,1 (mol)`
`=> n_[H_2] = 0,3 - 0,1 = 0,2 (mol)`
`b)m_[hh] = 0,2 . 56 + 0,1 . 88 = 20 (g)`

PTHH: Fe + 2HCl --> FeCl2 + H2
FeS + 2HCl --> FeCl2 + H2S
=> \(n_{Fe}+n_{FeS}=n_{H_2}+n_{H_2S}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Và 56.nFe + 88.nFeS = 18,8
=> \(\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{FeS}=0,15\left(mol\right)\end{matrix}\right.\)
Bảo toàn S: nCaSO3 = 0,15 (mol)
=> m = 0,15.120 = 18 (g)
=> B

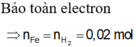
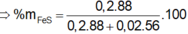
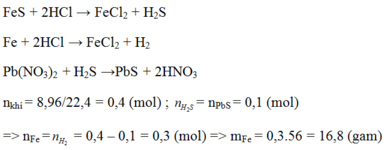
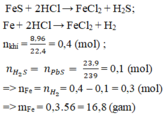
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> mFe = 0,2.56 = 11,2 (g)
\(n_{CuS}=\dfrac{9,6}{96}=0,1\left(mol\right)\)
PTHH: Cu(NO3)2 + H2S --> CuS + 2HNO3
0,1<---0,1
FeS + 2HCl --> FeCl2 + H2S
0,1<---------------------0,1
=> mFeS = 0,1.88 = 8,8 (g)
=> m = 11,2 + 8,8 = 20 (g)