cho 9,6 gam lưu huỳnh cháy trong không khí thu được khí lưu huỳnh đioxit a) viết phương trình phản ứng xảy ra b) tính khối lượng lưu huỳnh đioxit tạo thành c) tính thể tích không khí cần dùng, biết thể tích không khí bằng 5 lần thể tích khí oxi. Biết các khí đo ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nS = \(\dfrac{3,2}{32}=0,1mol\)
a)
PTHH: S + O2 -to--> SO2
0,1 0,1 0,1 (mol)
b) mSO2 = 0,1.64 = 6,4g
c) VO2 = 0,1.22,4 = 2,24 lít
Vkk = 5.VO2 = 5.2,24 = 11,2 lít

a) \(n_S=\dfrac{16}{32}=0,5\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,5->0,5------>0,5
=> mSO2 = 0,5.64 = 32 (g)
b) VO2 = 0,5.22,4 = 11,2 (l)
=> Vkk = 11,2.5 = 56 (l)
c)
\(n_{O_2}=\dfrac{24}{32}=0,75\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}< \dfrac{0,75}{1}\)
=> S hết, O2 dư
PTHH: S + O2 --to--> SO2
0,5->0,5------>0,5
=> nO2(dư) = 0,75 - 0,5 = 0,25 (mol)

nSO2 = 12,8 : 64=0,2 (mol)
pthh : S+ O2 -t->SO2
0,2<--0,2<------0,2(mol)
=> mS= 0,2.32=6,4 (g)
=> VO2= 0,2.22,4=4,48 (l)
ta có
VO2 = 1/5 Vkk <=> Vkk = VO2 : 1/5 = 4,48:1/5 = 22.4 (l)
S + O2 to→to→ SO2
nS=12,832=0,4(mol)
a) Theo PT: nSO2=nS=0,4(mol)
⇒VSO2=0,4×22,4=8,96(l)
b) Theo PT: nO2=nS=0,4(mol)
⇒VO2=0,4×22,4=8,96(l)
⇒VKK=5VO2=5×8,96=44,8(l)

a) PTHH : \(S+O_2->SO_2\)
b) Ta có : \(n_S\) = \(\dfrac{m_S}{M_S}\) = 0.1 (mol)
Có : \(n_S=n_{O_2}\)
--> \(n_{O_2}\) = 0.1 (mol)
=> \(V_{O_2\left(đktc\right)}\) = \(n_{O_2}\) . 22.4 = 2.24 (L)
\(n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\\ PTHH:S+O_2\underrightarrow{t^o}SO_2\\ \left(mol\right)..0,1\rightarrow0,1..0,1\\ V_{O_2}=0,1.22,4=2,24\left(l\right)\)

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít

a) Phương trình hóa học S + O2 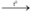 SO2
SO2
b) nS = 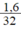 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 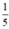 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l

a, \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
PTHH: S + O2 ----to----> SO2
Mol: 0,2 0,2 0,2
b, \(m_{SO_2}=0,2.64=12,8\left(g\right)\)
c, \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)

\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\\ pthh:S+O_2\underrightarrow{t^o}SO_2\)
0,3 0,3 0,3
\(m_{SO_2}=0,3.64=19,2\left(g\right)\\ V_{KK}=\left(0,3.22,4\right):\dfrac{1}{5}=33,6\left(L\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,3-->0,3----->0,3
\(\rightarrow\left\{{}\begin{matrix}m_{SO_2}=0,3.64=19,2\left(g\right)\\V_{kk}=0,3.5.22,4=33,6\left(l\right)\end{matrix}\right.\)