lên men m (g) tinh bột tạo thành rượu etylic toàn bộ khí co2 thu được hấp thụ vào ca(oh)2 sau pứ thấy thu được 30 g kết tủa và khối lượng dd giảm 12,4 (g).Biết hiệu suất của cả quá trình lên men là 75% xác định m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án C
Ta có sơ đồ:
(C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2![]() 2nCaCO3↓.
2nCaCO3↓.
ntinh bột = 1 mol
⇒ nCaCO3 = 1 × 2 × 0,75 = 1,5 mol
⇒ m = 1,5 × 100 = 150(g)

Đáp án D
nCaCO3 =0,8 mol → nCO2 =0,8 mol → theo lý thuyết nglucose= 0,4 mol
→ thực tế nglucozo= 0,4 :0,75 =0,53 mol
→ m=96

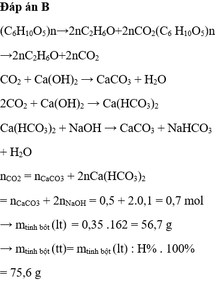
Đáp án B
Vì khi đun sôi dung dịch tạo thêm kết tủa chứng tỏ trong dung dịch có Ca(HCO3)2
Ca(OH)2 + CO2 → CaCO3 + H2O
Mol: 5,5 ← 550/100
Ca(HCO3)2 → t ° CaCO3 + CO2 + H2O
Mol: 1 ← 100/100
Bảo toàn nguyên tố C: nCO2 = nCaCO3 bđ + 2nCa(HCO3)2 = 5,5 + 2.1 = 7,5 mol
- Xét phản ứng lên men:
C6H10O5 + H2O → lên men 2CO2 + 2C2H5OH
Mol: 3,75 ← 7,5
nLT.H% = nThực => nLT.81% = 3,75 => nLT = 4,63 mol

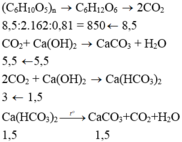

\(BTC:n_{CO_2}=n_{CaCO_3}=\dfrac{30}{100}=0,3mol\)
Lên men rượu:
\(\left(C_6H_{10}O_5\right)_n\rightarrow2nC_2H_5OH+2nCO_2\)
\(\dfrac{0,15}{n}\) 0,3
\(m_{ddgiảm}=m_{ktủa}-m_{CO_2}=12,4\)
\(\Rightarrow m_{CO_2}=30-12,4=17,6g\Rightarrow n_{CO_2}=\dfrac{17,6}{44}=0,4mol\)
Lượng tinh bột phản ứng:
\(m_{tinhbột}=162n\cdot\dfrac{0,15}{n}=24,3g\)
\(H=75\%\Rightarrow m=\dfrac{24,3}{75\%}\cdot100\%=32,4g\)