Đề: Đốt cháy hoàn toàn photpho trong bình chứa 1,12 lít oxi (đktc) thu được hợp chất có công thức P2O5 a, Viết phương trình hóa học ? b, Tính khối lượng sản phẩm thu được? c, Tính khối lượng kali clorat KClO3 cần dùng để điều chế được lượng oxi dùng trong phản ứng trên? ( Cho P=31 ; O =16 ; K=39 ; Mn=55 ; Cl = 35,5 ).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=0,1 mol
nO2=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g
2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=6,5/65=0,1 mol
n O2=0,8/32=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{1,55}{31}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,05}{4}>\dfrac{0,05}{5}\), ta được P dư.
c, Theo PT: \(n_{P\left(pư\right)}=\dfrac{4}{5}n_{O_2}=0,04\left(mol\right)\Rightarrow n_{P\left(dư\right)}=0,05-0,04=0,01\left(mol\right)\)
\(\Rightarrow m_{P\left(dư\right)}=0,01.31=0,31\left(g\right)\)

a.4Al + 3O2 -> 2Al2O3
0.8 0.6 0.4
\(nO2=\dfrac{19.2}{32}=0.6mol\)
b.mAl = \(0.8\times27=21.6g\)
c.mAl2O3 = \(0.4\times102=40.8g\)

a) 4Al + 3O2 --to--> 2Al2O3
b) \(n_{O_2}=\dfrac{19,2}{32}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,8<-0,6---------->0,4
=> mAl = 0,8.27 = 21,6(g)
c) mAl2O3 = 0,4.102 = 40,8(g)

Đáp án A
Dựa vào bản chất phản ứng của X với NaHCO 3 , bảo toàn nguyên tố O; bảo toàn electron trong phản ứng đốt cháy X, ta có :
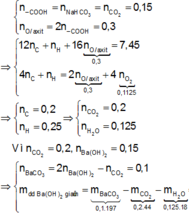
= 8,65 gam

a/ Ta có: \(n_{Mg}=\dfrac{4.8}{24}=0.2\left(mol\right)\)
PTHH:
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
2 1
0.2 x
\(=>x=\dfrac{0.2\cdot1}{2}=0.1=n_{O_2}\)
\(=>V_{O_2\left(đktc\right)}=0.1\cdot22.4=2.24\left(l\right)\)
b/ \(2Mg+O_2\underrightarrow{t^o}2MgO\)
2 2
0.2 y
\(=>y=\left(0.2\cdot2\right):2=0.2=n_{MgO}\)
\(=>m_{MgO}=0.2\cdot\left(24+16\right)=8\left(g\right)\)

Mg + 2HCl = MgCl2 +H2
x x
2Al + 6HCl= 2AlCl3 + 3H2
y y
2Cu + O2 = 2CuO
z z = 8/80 = 0,1 mol
3NaOH + AlCl3 = Al(OH)3 + 3NaCL
y y
Al(OH)3 + NaOH = NaALO2 + 2H2O
y y
2NaOH + MgCl2 = Mg(OH)2 + 2NaCl
x x
Mg(OH)2 = MgO + H2O
x x = 4/40 = 0,1 mol
=>mCu= 0,1*64=6,4
mMg=0,1*24=2,4
mAl=10-6,4-2,4=1,2


\(a) 4P+ 5O_2 \xrightarrow{t^o} 2P_2O_5\\ b) n_{O_2} = \dfrac{1,12}{22,4} = 0,05(mol)\\ n_{P_2O_5} = \dfrac{2}{5}n_{O_2} = 0,02(mol)\\ m_{P_2O_5} = 0,02.142 = 2,84(gam) c) 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{0,1}{3}(mol)\\ m_{KClO_3} = \dfrac{0,1}{3}122,5 = 4,083(gam)\)