Đốt cháy hoàn toàn 1,8 g một loại phân đạm A thu được 1,32 gam CO2 1,08 gam H2O Tính thành phần phần trăm khối lượng N trong A và 46,67% trong A ngoài C H Ncòn nguyên tố O a .cho biết phần trăm khối lượng các nguyên tố trong A b. lập công thức hóa học của A Biết rằng lượng Nitơ trong 1 mol A ít hơn lượng Nitơ trong 100 gam NH4NO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{1,32}{44}=0,03mol\Rightarrow n_C=0,03\Rightarrow m_C=0,36g\)
\(n_{H_2O}=\dfrac{0,54}{18}=0,03mol\Rightarrow n_H=0,06mol\Rightarrow m_H=0,06g\)
Nhận thấy \(m_C+m_H=0,42< m_A=0,9g\Rightarrow\)có chứa oxi.
\(\Rightarrow m_O=0,9-0,42=0,48g\)
Gọi CTHH là \(C_xH_yO_z\)
\(x:y:z=\dfrac{m_C}{12}:\dfrac{m_H}{1}:\dfrac{m_O}{16}=\dfrac{0,36}{12}:\dfrac{0,06}{1}:\dfrac{0,48}{16}=0,03:0,06:0,03\)
\(\Rightarrow x:y:z=1:2:1\Rightarrow CH_2O\)
Gọi CTPT là \(\left(CH_2O\right)_n\)
\(\Rightarrow M=180=30n\Rightarrow n=6\)
Vậy CTPT cần tìm là \(C_6H_{12}O_6\)

\(n_{CO_2}=\dfrac{5.28}{44}=0.12\left(mol\right)\Rightarrow n_C=0.12\left(mol\right)\Rightarrow m_C=0.12\cdot12=1.44\left(g\right)\)
\(n_{H_2O}=\dfrac{0.9}{18}=0.05\left(mol\right)\Rightarrow n_H=0.05\cdot2=0.1\left(mol\right)\)
\(n_{N_2}=\dfrac{0.224}{22.4}=0.01\left(mol\right)\Rightarrow n_N=0.02\left(mol\right)\Rightarrow m_N=0.02\cdot14=0.28\left(g\right)\)
\(m_O=m_A-m_C-m_H-m_N=2.46-1.44-0.1-0.28=0.64\left(g\right)\)
\(\%C=\dfrac{1.44}{5.28}\cdot100\%=27.27\%\)
\(\%H=\dfrac{0.1}{5.28}\cdot100\%=1.89\%\)
\(\%N=\dfrac{0.28}{5.28}\cdot100\%=5.3\%\)
\(\%O=65.54\%\)





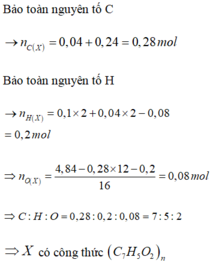

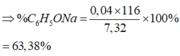
nCO2 = 0,03 mol → nC = nCO2 = 0,03 mol
nH2O = 0,06 mol → nH = 2nH2O = 0,12 mol
mN = 1,8.46,67% = 0,84 gam → nN = 0,84/14 = 0,06 mol
→ mO = mA - mC - mH - mN = 1,8 - 0,03.12 - 0,12 - 0,06.14 = 0,48 gam
→ nO = 0,48/16 = 0,03 mol
→ C : H : O : N = 0,03 : 0,12 : 0,03 : 0,06 = 1 : 4 : 1 : 2
→ CTPT có dạng (CH4ON2)n
Mà N trong 1 mol A ít hơn N trong 100 gam NH4NO3 nên ta có:
2n < 2.(100/80) → n < 1,25
→ n = 1
→ CTPT là CH4ON2 hay (NH2)2CO
Tên gọi của A là ure
Đoạn 2n<2(100/80) là sao ạ