Cho hòa tan hoàn toàn 10 g hỗn hợp 2 kim loại A và B vào dung dịch HCl thì thu được dung dịch C và khí H2. Cô cạn dung dịch C thu được 11,42 g muối khan. Tính thể tích khí H2 thu được ở đktc.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(5,41g\left\{{}\begin{matrix}Al\\Zn\end{matrix}\right.+HCl->\left\{{}\begin{matrix}AlCl3\\ZnCl2\end{matrix}\right.+H2\)
Ta có :
\(\left\{{}\begin{matrix}27x+65y=5,41\\133,5x+136y=17,48\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,08\\y=0,05\end{matrix}\right.\)
Bảo toàn e :
\(3x+2y=2.nH2\)
\(\Rightarrow nH2=0,17\left(mol\right)\)
\(\Rightarrow V=0,17.22,4=3,808\left(l\right)\)

Đáp án B
BTNT "H" ta có: nHCl = 2nH2 mol.
Đặt nH2 = x mol => nHCl = 2x mol
BTKL: m KL + mHCl = m muối + mH2
=> 5 + 2x.36,5 = 5,71 + 2x => x = 0,01
=> VH2 = 0,01.22,4 = 0,224 lit

a) \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
=> nHCl = 0,27 (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 5,85 + 0,27.36,5 - 0,135.2 = 15,435 (g)
b) VH2 = 3,024 (l) (Theo đề bài)
c)
Hỗn hợp kim loại gồm \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:3a\left(mol\right)\end{matrix}\right.\)
=> 27a + MX.3a = 5,85
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
X + 2HCl --> XCl2 + H2
3a------------------->3a
=> 1,5a + 3a = 0,135
=> a = 0,03 (mol)
=> MX = 56 (g/mol)
=> X là Fe

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
=> nHCl = 0,8 (mol)
Theo ĐLBTKL: mA,B + mHCl = mmuối + mH2
=> mA,B = 39,4 + 0,4.2 - 0,8.36,5 = 11 (g)

\(n_{H_2}=a\left(mol\right)\)
\(\text{Coi hỗn hợp là : kim loại M}\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(\text{Từ PTHH ta thấy : }\)
\(n_{HCl}=2n_{H_2}=2a\left(mol\right)\)
\(\text{Bảo toàn khối lượng : }\)
\(m_{hh}+m_{HCl}=m_{Muối}+m_{H_2}\)
\(\Leftrightarrow5+36.5\cdot2a=5.71+2a\)
\(\Leftrightarrow a=0.01\)
\(V_{H_2}=0.01\cdot22.4=0.224\left(l\right)\)
\(b.\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(FeO+H_2\underrightarrow{^{^{t^0}}}Fe+H_2O\)
\(n_{H_2O}=n_{H_2}=0.01\left(mol\right)\)
\(\text{Bảo toàn khối lượng : }\)
\(m_{hh}=m_{kl}+m_{H_2O}-m_{H_2}=0.6+0.01\cdot18-0.01\cdot2=0.76\left(g\right)\)

Đáp án D
Gọi M là kim loại chung cho Mg, Fe và Al với hóa trị n
Gọi số mol H2 thu được là a mol
Sơ đồ phản ứng :
![]()
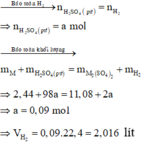

a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ \Rightarrow n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\\ Ta.có:m=m_{muối}=m_{kl}+\left(m_{HCl}-m_{H_2}\right)=11,2+\left(0,8.36,5-0,4.2\right)=39,6\left(g\right)\)
\(n_{H_2}=a\left(mol\right)\)
\(2A+2nHCl\rightarrow2ACl_n+nH_2\)
\(2B+2mHCl\rightarrow2BCl_m+mH_2\)
\(n_{HCl}=2n_{H_2}=2a\left(mol\right)\)
\(BTKL:\)
\(10+2a\cdot36.5=11.42+2a\)
\(\Rightarrow a=0.02\)
\(V_{H_2}=0.02\cdot22.4=0.448\left(l\right)\)