Hoang thành trương trình phản ứng sau, ghi rõ điều kiện phản ứng ( nếu có)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(c,Cl_2+Ca\left(OH\right)_2\underrightarrow{t^o}CaOCl_2+H_2O\\ d,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\\ h,Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\\ i,O_3+Ag\underrightarrow{t^o}Ag_2O+O_2\uparrow\)
Hoàn thành phương trình phản ứng thực hiện sơ đồ chuyển hóa sau đây(ghi rõ điều kiện xảy ra nếu có).

a)
\(Mg+\dfrac{1}{2}O_2\xrightarrow[]{t^o}MgO\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(MgCl_2+K_2CO_3\rightarrow2KCl+MgCO_3\downarrow\)
\(MgCO_3+2HNO_3\rightarrow Mg\left(NO_3\right)_2+H_2O+CO_2\uparrow\)
\(Mg\left(NO_3\right)_2+2KOH\rightarrow2KNO_3+Mg\left(OH\right)_2\downarrow\)
a) 2Mg + O2 ----------to---------> 2MgO
MgO + 2HCl -----------> MgCl2 + H2O
MgCl2 + K2CO3 ---------> MgCO3 + 2KCl
MgCO3 + 2HNO3 --------> Mg(NO3)2 + H2O + CO2
Mg(NO3)2 + 2KOH ----------> Mg(OH)2 + 2KNO3

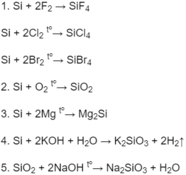
1) S+ O2 -t--> SO2(phản ứng hoa hợp)
2) 4P+5O2--t--> 2P2O5 (phản ứng hóa hợp )
3) 3Fe+ 2O2 --t--> Fe3O4 (phản ứng hóa hợp )
4) CH4 + 2O2 --> CO2+2H2O ( phản ứng xãy ra sự Oxi hóa)
5 ) 2KMnO4 --t--> K2MnO4 + MnO2+O2 (phản ứng phân hủy)
6) 2H2 + O2 ----> 2H2O(phản ứng hóa hợp )
7) CuO+H2 --t---> Cu +H2O(Phản ứng oxi hóa -khử)
8) Zn + 2HCl ----> ZnCl2 + H2(phản ứng thế)
(1) S + O2 --->(to) SO2 : pứ hóa hợp
(2) 4P + 5O2 --->(to) 2P2O5 : pứ hóa hợp
(3) 3Fe + 2O2 --->(to) Fe3O4 : pứ hóa hợp
(4) CH4 + 2O2 --->(to) CO2 + 2H2O : pứ oxi hóa
(5) 2 KMnO4 --->(to) K2MnO4 + MnO2 + O2 : pứ phân hủy
(6) 2H2 + O2 --->(to) 2H2O : pứ hóa hợp
(7) CuO + H2 --->(to) Cu + H2O : pứ oxi hóa-khử
(8) Zn + 2HCl ---> ZnCl2 + H2 : pứ thế

2.
\(\left(1\right)2KClO_3\underrightarrow{t^0}2KCl+3O_2\left(phản.ứng.phân,huỷ\right)\\ \left(2\right)2Al+3H_2SO_4\xrightarrow[]{}Al_2\left(SO_4\right)_3+3H_2\left(phản.ứng.thế\right)\\ \left(3\right)Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\left(phản.ứng.thế\right)\\ \)
(1) Điều chế O2 trong phòng thí nghiệm.
(2), (3) Điều chế H2 trong phòng thí nghiệm.
3.
\(a.\\ n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\\ PTHH:K+H_2O\xrightarrow[]{}KOH+H_2\\ \Rightarrow n_K=n_{H_2}=n_{KOH}=0,2mol\\ V_{H_2}=0,2.22,4=4,48\left(l\right)\\ b.\\ m_{KOH}=0,2.56=11,2\left(g\right)\)
Khi nhúng quì tím vào dung dịch, dung dịch làm quì tím chuyển thành màu xanh.

\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\\ 2H_2+O_2\underrightarrow{t^o}2H_2O\\ SO_3+H_2O\rightarrow H_2SO_4\)

Zn + H2SO4 --> Z+nSO4 + H2 (phản ứng thế)
H2 + CuO --> Cu + H2O (50độ) ( phản ứng khử oxit kim loại)

\(CH_2=CH_2+H_2O\rightarrow\left(H_2SO_4,t^o\right)CH_3CH_2OH\\ CH_3CH_2OH+CH_3COOH⇌\left(H^+,t^o\right)CH_3COOC_2H_5+H_2O\)

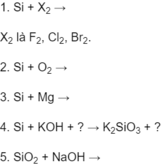
Câu 29.
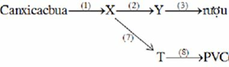
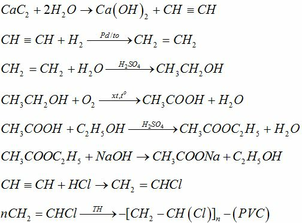
\(C_4H_{10}\rightarrow CH_4+C_3H_6\)
\(2CH_4\xrightarrow[1500^oC]{làmlạnhnhanh}C_2H_2+2H_2\uparrow\)
\(C_2H_2+HCl\xrightarrow[xtHgCl_2]{t^o,p}C_2H_3Cl\)
Câu 30.
\(n_{hh}=\dfrac{4,48}{22,4}=0,2mol\)
\(C_3H_4+2Br_2\rightarrow C_3H_4Br_4\)
\(n_{Br_2}=\dfrac{32}{160}=0,2mol\Rightarrow n_{C_3H_4}=0,1mol\)
\(\Rightarrow n_{CH_4}=0,2-0,1=0,1mol\)
a)\(\%m_{C_3H_4}=\dfrac{0,1\cdot40}{0,1\cdot40+0,1\cdot16}\cdot100\%=71,43\%\)
\(\%m_{CH_4}=100\%-71,43\%=28,57\%\)
b)Dẫn 4,48l hỗn hợp qua dung dịch \(AgNO_3\)/\(NH_3\) thì chỉ có \(C_3H_4\) phản ứng.
\(C_3H_4+AgNO_3+NH_3\rightarrow AgC\equiv C-CH_3\downarrow+NH_4NO_3\)
0,1 \(\rightarrow\) 0,1
\(m_{\downarrow}=0,1\cdot147=14,7g\)
Giúp mik hoàn thành phương trình nhé( với lại mik bấm lộn phải phương trình ko Pk trương trình đou)