Chia 20 g hỗn hợp X gồm Al , Fe , Cu thành 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch HCl đặc dư thu được 5,6 lit khí (dktc). Phần 2 cho tác dụng với dung dịch NaOH dư thu được 3,36 lit khí (dktc). Phần trăm khối lượng Cu trong hỗn hợp là :
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phần 1
2Al +6 HCl ----> 2AlCl3 + 3H2 (1)
Fe + 2HCl ----> FeCl2 + H2 (2)
Cu ko pư với dd HCl
Phần 2
2Al + 2NaOH + 2H20 ---> 2NaAlO2 + 3H2 (3)
Fe và Cu ko pư với dd NaOH
Theo pt(3) n Al = \(\frac{2}{3}\).n H2=\(\frac{2}{3}\). \(\frac{3,36}{22,4}\)=0,1 (mol)
%m Al= \(\frac{0,1.27}{20}\).100%= 13,5%
Theo pt(1)(2) tổng n H2=\(\frac{3}{2}\). nAl + n Fe=\(\frac{5,6}{22,4}\)
==> 0,15 + n Fe = 0,25 ==> n Fe = 0,1 (mol)
%m Fe= \(\frac{0,1.56}{20}\).100%= 28%
%m Cu=100% - 13,5% - 28% =58,5%
tại sao % Al lại đem chia 20 vậy 0,1 mol là ở 1 phần thôi là chia 10 chứ .% Fe cũng thế vậy
==> tổng mAl + mFe trong 1 phần = 0,1.27 + 0,1.56=8,3
%Cu =100% - \(\dfrac{8,3}{10}\).100=17%

a)
Gọi số mol Fe, Al, Ag trong mỗi phần là a, b,c (mol)
=> 56a + 27b + 108c = 5,19 (1)
Phần 1:
\(n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----->a------------------>a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b------>1,5b------------------->1,5b
=> a + 1,5b = 0,105 (2)
Phần 2:
\(n_{SO_2}=\dfrac{2,912}{22,4}=0,13\left(mol\right)\)
PTHH: 2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
b----->3b-------------------->1,5b
2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------>3a--------------------->1,5a
2Ag + 2H2SO4 --> Ag2SO4 + SO2 + 2H2O
c-------->c------------------>0,5c
=> 1,5a + 1,5b + 0,5c = 0,13 (3)
(1)(2)(3) => a = 0,03 (mol); b = 0,05 (mol); c = 0,02 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=2.0,03.56=3,36\left(g\right)\\m_{Al}=2.0,05.27=2,7\left(g\right)\\m_{Ag}=2.0,02.108=4,32\left(g\right)\end{matrix}\right.\)
b)
- Phần 1:
\(n_{H_2SO_4}=a+1,5b=0,105\left(mol\right)\)
- Phần 2:
\(n_{H_2SO_4}=3a+3b+c=0,26\left(mol\right)\)

Đáp án : D
Gọi số mol Al ; Zn ; Fe lần lượt là x ; y ; z
=> 27x + 65y + 56z = 20,4 (1)
Và 1,5x + y + z = nH2 = 0,45 (2)
Xét 0,2 mol X có lượng chất gấp t lần 20,4g X
=> t(x + y +z) = 0,2 mol (3)
Lại có : Bảo toàn e : 2nCl2 = (3x + 2y + 3z)t = 0,55 (4)
Từ (1),(2),(3),(4) => x = y = 0,1 ; z = 0,2
=> %mAl(X) = 13,24%

\(\text{Mỗi phần,gọi :} n_{Al} = a ; n_{Fe} = b ; n_{Cu} = c\\ \Rightarrow 27a + 56b + 64c = \dfrac{35,8}{2} = 17,9(1)\\ \text{Phần 1 : Al,Fe không phản ứng với axit đặc nguội}\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O\\ n_{Cu} = c = n_{SO_2} = \dfrac{3,36}{22,4} = 0,15(2)\\ \text{Phần 2 : Cu không phản ứng với axit loãng}\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(3)\\ (1)(2)(3) \Rightarrow a = b = 0,1 ; c = 0,15\)
Suy ra :
\(m_{Al} = 0,1.2.27 = 5,4(gam)\\ m_{Fe} = 0,1.2.56 = 11,2(gam)\\ m_{Cu} = 0,15.64.2 = 19,2(gam)\)

P1 :\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: nH2 = nFe = 0,1 mol
P2 :2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O (1)
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O (2)
Ta có: \(\dfrac{3}{2}.0,1\) + nSO2(2) = 0,4 mol
=> x = 0,1 ; y = 0,25 mol
Do chia 2 hỗn hợp X thành phần bằng nhau nên trong gam X có: 0,2 mol Fe và 0,5 mol Cu
=> \(\%m_{Fe}=\dfrac{0,2.56}{0,2.56+0,3.64}.100=36,84\%\)
%m Cu=63,16%
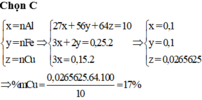
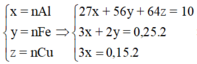
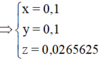
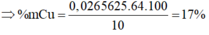


Xét P2 : Chỉ có Al phản ứng với NaOH => nAl.3 = 2nH\(_2\) ( Bảo toàn e)
=> nAl = 0,1 mol
Xét P1 : Fe và Al phản ứng với HCl đặc => 2nFe + 3nAl = 2nH\(_2\)
=> nFe = 0,1 mol
=> Trong mỗi phần thì có : mCu = \(\dfrac{1}{2}.10-27.0,1-56.0,1=1,7\left(g\right)\)
\(\%m_{Cu\left(X\right)}=\%m_{Cu\left(1/2X\right)}=17\%\)