Người ta dùng 120 tấn quặng pirit có chứa 10% tạp chất để sản xuất Fe ta thu được 48. tấn sắt. Tính hiệu suất phản ứng trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


mtạp chất=120.10%=12(tấn)
mFeS2=120-12=108(tấn)
mFe lý thuyết=\(\dfrac{108}{120}.56=50,4\left(tấn\right)\)
H=\(\dfrac{48}{50,4}.100\%=95,238\%\)

\(n_{Fe} = \dfrac{5000.1000}{56} = \dfrac{625000}{7}\ kmol\\ n_{FeS_2\ đã\ dùng} = \dfrac{n_{Fe}}{H\%} = \dfrac{\dfrac{625000}{7}}{89,6\%} = 99649,23\ kmol\\ m_{quăng\ pirit} = \dfrac{m_{FeS_2}}{90\%} = \dfrac{99649,23.120}{90\%} = 13259897,33 (kg) = 13259,89(tấn)\)
\(n_{Fe}=\dfrac{5000\cdot10^6}{56}=\dfrac{625}{7}\cdot10^6\left(mol\right)\)
\(BTFe:\)
\(n_{FeS_2}=n_{Fe}=\dfrac{625}{7}\cdot10^6\left(mol\right)\)
\(n_{FeS_2\left(tt\right)}=\dfrac{\dfrac{625}{7}\cdot10^6}{89.6}=\dfrac{56000\cdot10^6}{7}\left(mol\right)\)
\(\Rightarrow m_{FeS_2}=\dfrac{56000\cdot10^6\cdot120}{7}=960000\cdot10^6\left(g\right)=960000\left(tấn\right)\)
\(m_{quặng}=\dfrac{960000\cdot100}{90}=1066666.67\left(tấn\right)\)

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
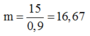

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.


K/lượng của Fe2O3 nguyên chất trong 250 tấn quặng hematit là :
250.60%=150(tấn)
=150000000(g)
Fe2O3+3CO-->2Fe+3CO2
Số mol của Fe2O3 là:
n=m/M=150000000:160
=937500(mol)
Số mol của Fe là:
nFe=2nFe2O3=2.937500
=1875000(mol)
K/lượng của Fe là:
m=n.M=1875000.56
=105000000(g)
K/lượng của Fe nếu hiệu suất chỉ đạt 90% là:
105000000.90%
=94500000(g)
=94,5 tấn
Mình không biết là đúng hay sai nha
Cảm ơn bạn nka! Nhưng tiếc là mình đã hoàn thành bài này xong rồi.

Đáp án C.
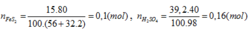
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%


Cái này là vật lí sao đăng trên này chi
giúp mình với mọi người!!!!