Lắc m gam bột Fe với dung dịch A gồm AgNO3 và Cu(NO3)2 đến khi phản ứng kết thúc thu được x gam chất rắn B. Tách B thu được nước lọc C. CHo nước lọc C tác dụng với dd NaOH dư thu được a gam kết tủa của 2 Hidroxit kim loại. Nung kết tủa trong kk đến khối lượng không đổi thu được b gam chất rắn. 1. Lập biểu thức tính m theo a và b. 2.Cho a=36,8; b=32; x= 34,4 gam. Tính giá trị m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Bài này có thể giải theo kinh nghiệm,
hoặc biện luận rào số mol hỗn hợp A.
Từ đó ⇒ giới hạn của chất rắn C
Trường hợp xả ra đó là:
Fe pứ hết và Cu chỉ pứ 1 phần
⇒ C gồm Ag và Cu chưa tan.
+ Sơ đồ ta có:
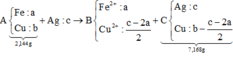

PT theo khối lượng oxit:
40c = 2,56 Û c = 0,064 mol
⇒ CM AgNO3 = 0,064 ÷ 0,2 = 0,32

Bài này có thể giải theo kinh nghiệm, hoặc biện luận rào số mol hỗn hợp A.
Từ đó ⇒ giới hạn của chất rắn C
Trường hợp xả ra đó là:
Fe pứ hết và Cu chỉ pứ 1 phần ⇒ C gồm Ag và Cu chưa tan.
+ Sơ đồ ta có:
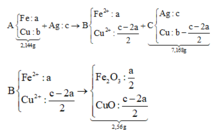
PT theo khối lượng oxit: 40c = 2,56 Û c = 0,064 mol
⇒ CM AgNO3 = 0,064 ÷ 0,2 = 0,32
Đáp án A

Đáp án C
Sau phản ứng thu được hỗn hợp kim loại C => Chứng tỏ C chứa Ag, Cu, có thể có Fe dư, Al dư.
Có khối lượng chất rắn thu được ở phần 1 nhiều hơn phần 2 => Chứng tỏ trong dung dịch ngoài Al(NO3)3 còn chứa Fe(NO3)2
=> Al, Cu(NO3)2 và AgNO3 phản ứng hết, Fe có thể còn dư.
Đặt số mol Cu(NO3)2 và AgNO3 lần lượt là a, b.
Đặt số mol Al và Fe phản ứng lần lượt là x, ỵ
Chất rắn thu được ở phần 2 là Fe2O3 => 160.0,5y = 6,2 => y = 0,15
Chất rắn thu được ở phần 1 là Al2O3 và Fe2O3
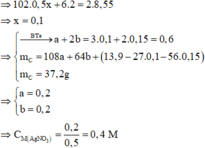



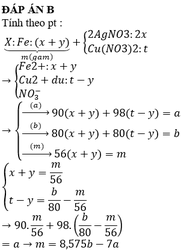
bn tk luôn tính độ mol hén