Bài 18. Cho 35,411 gam hỗn hợp A gồm muối natri của hai halogen ở hai chu kì liên tiếp trong BTH tác dụng với dung dịch AgNO3 dư thu được 68,306 gam kết tủa.
a. Tìm tên hai halogen. b. Tính khối lượng từng muối trong hỗn hợp A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+) Trường hợp 1: Hỗn hợp gồm NaF và NaCl
PTHH: \(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
Ta có: \(n_{AgCl}=\dfrac{2,87}{143,5}=0,02\left(mol\right)=n_{NaCl}\)
\(\Rightarrow m_{NaCl}=0,02\cdot58,5=1,17\left(g\right)\) \(\Rightarrow m_{NaF}=0,415\left(g\right)\)
+) Trường hợp 2: Hỗn hợp không chứa NaF
Gọi công thức chung 2 muối là NaR
PTHH: \(NaR+AgNO_3\rightarrow NaNO_3+AgR\downarrow\)
Theo PTHH: \(n_{NaR}=n_{AgR}\) \(\Rightarrow\dfrac{1,595}{23+\overline{M}_R}=\dfrac{2,87}{108+\overline{M}_R}\)
\(\Rightarrow\overline{M}_R\approx83,3\) \(\Rightarrow\) 2 halogen cần tìm là Brom và Iot
Vậy 2 muối có thể là (NaF và NaCl) hoặc (NaBr và NaI)
*P/s: Các phần còn lại bạn tự làm

Chọn A
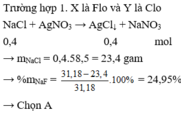
Chú ý: Với đề trắc nghiệm chọn được đáp án A có thể không cần xét thêm trường hợp 2.
Trường hợp 2. X khác Flo. Gọi hỗn hợp (NaX, NaY) tương đương với NaM


Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br

Đáp án D
Trường hợp 1: Hai halogen đều tạo được kết tủa với AgNO3
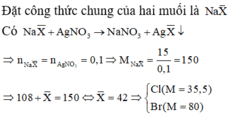
Do đó hai muối trong X là NaCl và NaBr
Trường hợp 2: Hai muối là NaF và NaCl
Phản ứng tạo thành kết tủa chỉ có AgCl và AgF là muối tan:
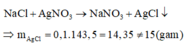
Do đó trường hợp này không thỏa mãn.

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
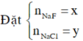
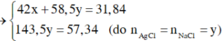
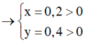
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
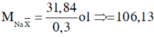
=> 2 muối là NaBr và NaI
Đáp án A

Chia làm 2 trường hơp:
TH1: Giả sử cả 2 halogen đều tạo kết tủa với bạc.
Gọi công thức trung bình của 2 halogen là NaX:
NaX + AgNO3 ---> AgX (kết tủa) + NaNO3
3,87 170x 6,63 85x
Áp dụng định luật bảo toàn khối lượng ta có: 3,87 + 170x = 6,63 + 85x
Suy ra số mol phản ứng: x = 0,03247 mol.
Nguyên tử khối trung bình của 2 halogen là: X = 3,87/0,03247 - 23 = 96,18.
Như vậy 2 halogen cần tìm là Brom (80) và Iot (127).
TH2: Giả sử chỉ có 1 halogen tạo kết tủa với bạc, halogen còn lại không tạo kết tủa với bạc là Flo.
Vì 2 halogen liên tiếp nên halogen còn lại là Clo.
NaCl + AgNO3 ---> AgCl + NaNO3
nNaCl = nAgCl = 6,63/143,5 = 0,0462 mol.
mNaCl = 0,0462.58,5 = 2,7 g.
mNaF = 3,87 - 2,7 = 1,17 g.

Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)
- Nếu một trong 2 muối là NaF => Muối còn lại là NaCl
\(n_{AgCl}=\dfrac{68,306}{143,5}=0,476\left(mol\right)\)
PTHH: NaCl + AgNO3 --> NaNO3 + AgCl
0,476<-----------------------0,476
=> mNaCl = 0,476.58,5 = 27,846(g)
=> mNaF = 35,411 - 27,846 = 7,565(g)
- Nếu trong A không có NaF
=> Gọi công thức của 2 muối là NaX
=> \(n_{NaX}=\dfrac{35,411}{23+M_X}\left(mol\right)\)
PTHH: NaX + AgNO3 --> NaNO3 + AgX
\(\dfrac{35,411}{23+M_X}\)----------------->\(\dfrac{35,411}{23+M_X}\)
=> \(\dfrac{35,411}{23+M_X}=\dfrac{68,306}{108+M_X}\)
=> \(M_X=68,5\)
=> 2 muối là NaCl, NaBr
Gọi số mol của NaCl, NaBr là a, b
=> 58,5a + 103b = 35,411
PTHH: NaCl + AgNO3 --> AgCl + NaNO3
a------------------>a
NaBr + AgNO3 --> AgBr + NaNO3
b------------------->b
=> 143,5a + 188b = 68,306
=> a = 0,1; b = 0,287
=> \(\left\{{}\begin{matrix}m_{NaCl}=0,1.58,5=5,85\left(g\right)\\m_{NaBr}=0,287.103=29,561\left(g\right)\end{matrix}\right.\)