Tính thể tích O2(đktc) cần dùng để đốt cháy hoàn toàn 67,2 lít khí chứa 25% tạp chất không cháy. Các thể tích đo ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(V_{CH_4(nguyên chất)}=1000.98\%=980(l)\\ \Rightarrow n_{CH_4}=\dfrac{980}{22,4}=43,75(mol)\\ CH_4+2O_2\xrightarrow{t^o}CO_2+2H_2O\\ \Rightarrow n_{O_2}=87,5(mol)\\ \Rightarrow V_{O_2}=87,5.22,4=1960(l)=1,96(m^3)\)

Ta có: 1 m3 = 1000 dm3 = 1000 lít
Trong 1 m3 có chứa 2% tạp chất nên lượng khí CH4 nguyên chất là:
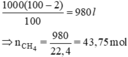
Phương trình phản ứng:
CH4 + 2O2 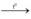 CO2 + 2H2O
CO2 + 2H2O
Từ phương trình ta có: nO2 = 2nCH4 = 2.43,75 = 87,5 mol
⇒ VO2 = 87,5.22,4= 1960 lít

V(C4H10,đktc)= 44,8. 98%= 43,904(l)
PTHH: 2 C4H10 + 13 O2 -to-> 8 CO2 + 10 H2O
Vì số mol tỉ lệ thuận với thể tích, nên ta có:
V(O2,đktc)= 13/2 . V(C4H10,đktc)= 13/2 . 43,904= 285,376(l)

CH4 + 2O2 ---to--> CO2 + 2H2O
nCH4 = 4,48 : 22,4 = 0,2 (mol)
--> VO2 = 0,2 x 2 x 22,4 = 8,96 (l)
--> Vkk = 8,96 x 5 = 44,8 (l)
nhá


\(Ta.có.trong.kk.có.78\%N_2,21\%O_2,1\%.là.các.khí.khác\)
\(\Rightarrow O_2.tác.dụng.với.N_2\left(do.O_2.ko.tác.dụng.với.O_2.và.thể.tích.sinh.ra.khi.O_2.tác.dụng.với.các.khí.khác.và.3\%N_2.ko.đáng.kể\right)\)\(V_{N_2\left(đktc\right)}=V_{kk\left(đktc\right)}.75\%=67,2.75\%=50,4\left(l\right)\\ n_{N_2}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{50,4}{22,4}=2.25\left(mol\right)\\ PTHH:2O_2+N_2\underrightarrow{t^o}2NO_2\\ Theo.PTHH:n_{O_2}=2.n_{N_2}=2.2,25=4,5\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=4,5.22,4=100,8\left(l\right)\)
đốt cháy cái j v