Nung 200 gam CaCO 3 , Sau một thời gian ta thu được chất rắn có khối lượng 129,6 gam . Hỏi thể tích khí CO 2 sinh ra ( ở đktc ) là bao nhiêu lít?( Ca=40, C=12 , O=16)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(BTKL\)
\(m_{O_2}=20-18.08=1.92\left(g\right)\)
\(n_{O_2}=\dfrac{1.92}{32}=0.06\left(mol\right)\)
\(V_{O_2}=0.06\cdot22.4=1.344\left(l\right)\)
- Thấy sau phản ứng chỉ có khí O2 thoát ra làm giảm khối lượng củ hỗn hợp.
=> mtrc - ms = mO2 = 1,92g
=> nO2 = 0,12 mol
=> V = 2,688l

Đáp án C
Hướng dẫn giải:
NH4NO3 → N2O + 2H2O
x x 2x mol
Khối lượng chất rắn giảm chính là do N2O và H2O bay hơi
→mN2O+ mH2O= 44x + 2x.18= 80x = 40-10=30 gam → x= 0,375 mol
→Vkhí và hơi= 3x.22,4=25,2 lít

a, nCO2 = 0,06 ( mol )
=> nCO = 0,06 ( mol )
ADĐLBTKL : \(m_{CO}+m_{Fe2O3}=m_{hh}+m_{CO_2}\)
=> \(m=m_{Fe2O3}=5,44+0,06.44-0,06.28=6,4\left(g\right)\)
b, nCO2 lấy = 0,012 ( mol )
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
.0,002........0,002........0,002...............
=> nCO2 còn lại = 0,012 - 0,002 = 0,01 ( mol )
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
......0,005.......0,01........0,005.......
\(Ca\left(HCO_3\right)_2\rightarrow CaCO_3+H_2O+CO_2\) ( * )
...0,005..............0,005................
=> Tổng nCa(OH)2 = 0,002 + 0,005 = 0,007 ( mol )
=> CMCa(OH)2 = 0,014M .
=> m1 = mCaCO3 (*) = 0,5 ( g )
Vậy ...

a) \(n_{KCl}=\dfrac{14,9}{74,5}=0,2\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,2<-----------0,2----->0,3
=> mKClO3 = 0,2.122,5 = 24,5(g)
VO2 = 0,3.22,4 = 6,72(l)
b) \(n_{KClO_3}=\dfrac{25,725}{122,5}=0,21\left(mol\right)\)
Gọi số mol KClO3 pư là a
=> (0,21-a).122,5 + 74,5a = 16,125
=> a = 0,2 (mol)
=> nO2 = 0,3 (mol)
=> VO2 = 0,3.22,4 = 6,72(l)

a, PTHH: 2KClO3 --to--> 2KCl + 3O2
b, \(n_{O_2}=\dfrac{53,76}{22,4}=2,4\left(mol\right)\\ n_{O_2}=2,4.32=76,8\left(g\right)\)
Bảo toàn khối lượng: \(m_{KClO_3}=76,8+168,2=245\left(g\right)\)
c, Theo pthh: \(n_{KClO_3\left(pư\right)}=\dfrac{2}{3}n_{O_2}=\dfrac{2}{3}.2,4=1,6\left(mol\right)\\ \Rightarrow\%m_{KClO_3\left(phân.huỷ\right)}=\dfrac{1,6.122,5}{245}=80\%\)

a. pứ: CaCO3 ------> CaO + CO2
b. nCaCO3 = \(\dfrac{15}{100}\)= 0,15 mol
từ phương trình ta suy ra được:
nCaO = nCaCO3 = 0,15 mol
mCaO= 0,15 . 56 = 8,4 g
c. theo phương trình:
nCO2 = nCaO = 0,15 mol
VCO2 = 0,15 . 22,4 = 3,36 (lít)

Tóm tắt: 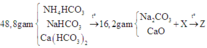
Gọi a; b; c lần lượt là số mol của NH4HCO3, NaHCO3 và Ca(HCO3)2
Ta có: 89a + 84b + 162c =48,8 (l)
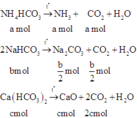
Khối lượng của hỗn hợp rắn là: 53b + 56c = 16,2 (2)
Hỗn hợp khí X gồm NH3 (a mol) và CO2 (a + b 2 + 2c)
⇒ n x = (2a + b 2 + 2c)
Khi X ở nhiệt độ 180 – 200°C, dưới áp suất khoảng 200 atm thì đây chính là phản ứng điều chế đạm urê nên ta có phản ứng:
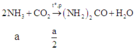
NH3 phản ứng với CO2 theo tỉ lệ 1:2 lượng khí Z còn lại chính là CO2 ⇒ n z = a 2 + b 2 . 2 c
Do sau phản ứng đưa về nhiệt độ ban đầu nên ta có:
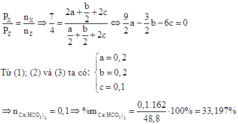
Đáp án A.
\(n_{CaCO_3}=\dfrac{200}{100}=2\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
_______a-------------->a----->a
=> 100(2-a) + 56a = 129,6
=> a = 1,6 (mol)
=> VCO2 = 1,6 .22,4 = 35,84(l)
a giải thích cho em chỗ 100(2-a) + 56a =129,6 được không ạ