Cho 4,64 gam một oxit sắt tác dụng với lượng dư khí H2, lượng kim loại sinh ra đem phản ứng với dd Cu(NO3)2 dư thì thấy sinh ra 3,84 gam kim loại. Gọi tên oxi sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)

\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1---->0,3
Zn + H2SO4 --> ZnSO4 + H2
0,3<--------------------0,3
=> m = 0,3.65 = 19,5 (g)

`a)`
Oxit: `Fe_xO_y`
`Fe_xO_y+yCO` $\xrightarrow{t^o}$ `xFe+yCO_2`
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
Theo PT: `n_{CO_2}=n_{CaCO_3}=7/{100}=0,07(mol)`
`->n_{Fe_xO_y}={n_{CO_2}}/y={0,07}/y(mol)`
`->M_{Fe_xO_y}={4,06}/{{0,07}/y}=58y`
`->56x+16y=58y`
`->x/y={42}/{56}=3/4`
`->` Oxit: `Fe_3O_4`
`b)`
`n_{Fe_3O_4}={4,06}/{232}=0,0175(mol)`
`2Fe_3O_4+10H_2SO_4->3Fe_2(SO_4)_3+SO_2+10H_2O`
Đề thiếu.

Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+2HCl--->FeCl_2+H_2\left(1\right)\)
\(CuO+H_2\overset{t^o}{--->}Cu+H_2O\left(2\right)\)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(lít\right)\)
b. Ta thấy: \(\dfrac{0,15}{1}< \dfrac{0,2}{1}\)
Vậy CuO dư.
Theo PT(2): \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)

Đáp án A
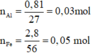
Sau phản ứng thu được 3 kim loại => Fe còn dư; Al, AgNO3 và Cu(NO3)2 đều phản ứng hết; 3 kim loại thu được gồm Ag, Cu và Fe dư.
![]()
Đặt số mol của AgNO3 và Cu(NO3)2 lần lượt là a, b
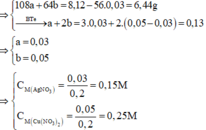



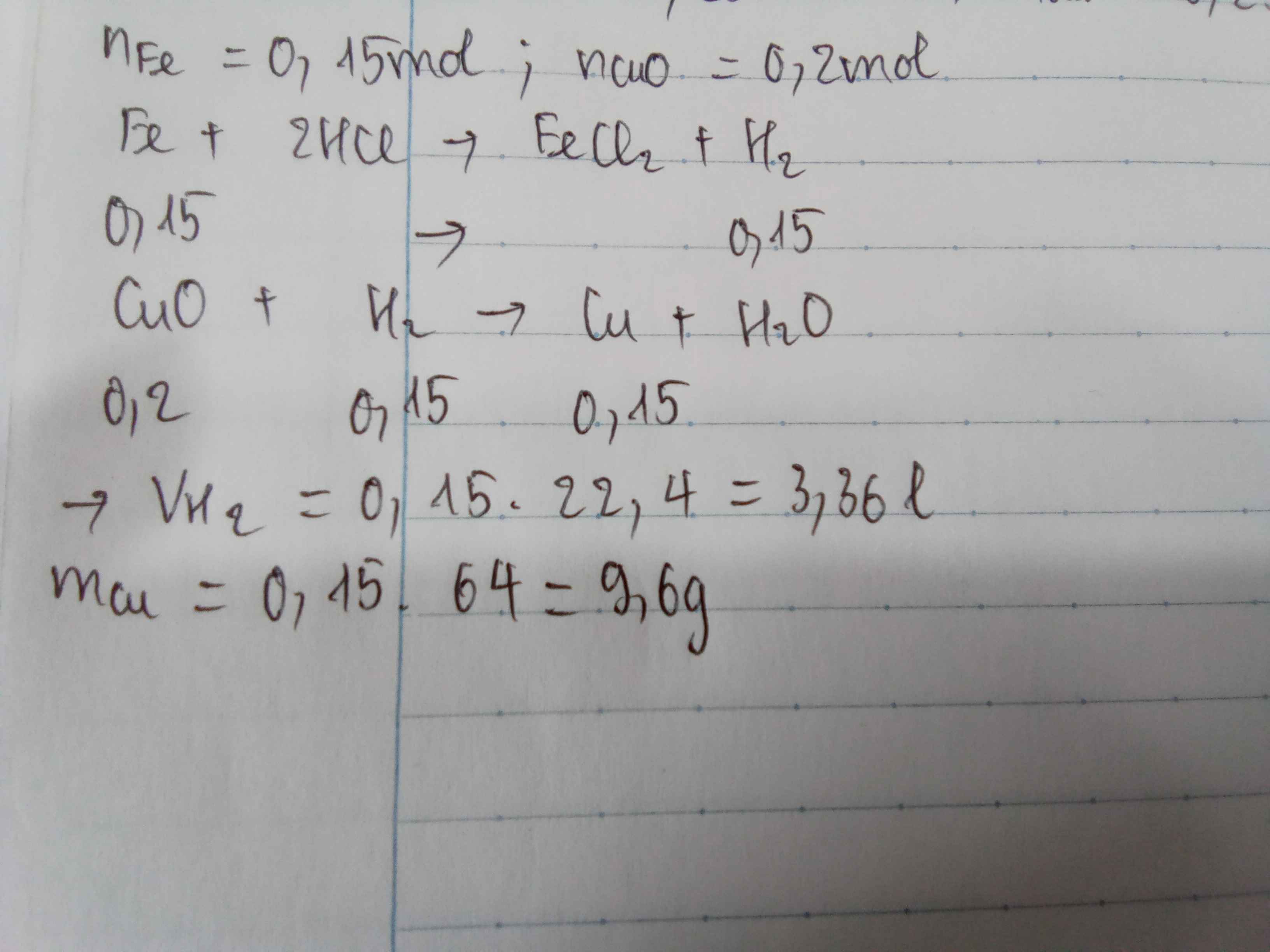

\(n_{Cu}=\dfrac{3,84}{64}=0,06\left(mol\right)\)
CTHH: FexOy
PTHH: Fe + Cu(NO3)2 --> Fe(NO3)2 + Cu
_____0,06<--------------------------------0,06
FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,06}{x}\)<----------------0,06
=> \(M_{Fe_xO_y}=\dfrac{4,64}{\dfrac{0,06}{x}}=\dfrac{232}{3}.x\left(g/mol\right)\)
=> x = 3 => y = 4
=> CTHH: Fe3O4