chia m gam hỗn hợp al, mg làm 2 phần : phần 1: cho tác dụng hết với 400 ml dung dịch hci 0,3m thu được v lít khi (đktc) phần 2: cho tác dụng hết với dung dịch hno, dư thu được 672ml khi ng0 (dktc) và dung dịch a. cho dung dịch a tác dụng hết với dung dịch nh3 dư thu được 6,6g kết tủa. a) tinh thành phần phần trãm khối lượng mỗi kim loại trong hỗn hợp b) tinh v
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).

Đáp án A
Tương tự Câu 12, áp dụng định luật bảo toàn mol electron ta có
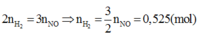
Vậy V= 11,76 (lít)

Đáp án A
Tương tự câu 12, áp dụng định luật bảo toàn mol electron ta có:
2 n H 2 = 3 n N O = > 3 2 n N O = 0 , 525 ( m o l )
Vậy V = 11,76 (lít)

Đáp án A
Có
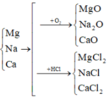
Vì các kim loại trong hỗn hợp X có hóa trị không đổi và khối lượng mỗi phần đều là 11 gam nên số mol electron trao đổi ở mỗi phần là như nhau.
Áp dụng định luật bảo toàn khối lượng ta có:
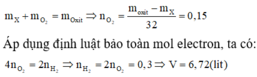

Đáp án B
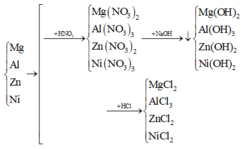
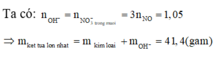
Khối lượng hỗn hợp mỗi phần là 23,55 gam.
Vì để thu được khối lượng kết tủa là lớn nhất nên không có sự hòa tan kết tủa bởi NaOH dư.

Đáp án B

Khối lượng hỗn hợp mỗi phần là 23,55 gam.
Vì để thu được khối lượng kết tủa là lớn nhất nên không có sự hòa tan kết tủa bởi NaOH dư.
Ta có:
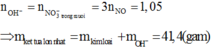
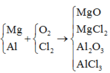
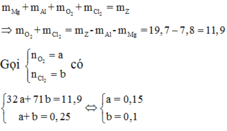
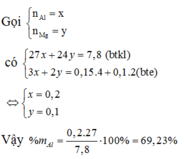
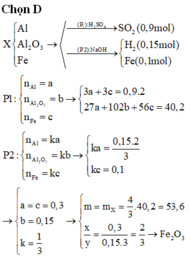
Ng0 là n20 nha