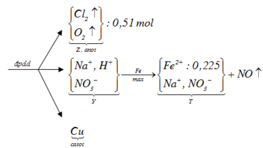
Điện phân điện cực trơ màng ngăn xốp, dung dịch X chứa a gam Cu(NO3)2 và b gam NaCl đến khi có khí thoát ra ở cả 2 điện cực thì dừng lại, thu được dung dịch Y và 0,51 mol khí Z. Dung dịch Y hòa tan tối đa 12,6 gam Fe giải phóng NO (sản phẩm khử duy nhất) và dung dịch T. Dung dịch T cho kết tủa với dung dịch AgNO3. Tổng giá trị của (a + b) là
A. 135,36.
B. 147,5.
C. 171,525
D. 166,2.

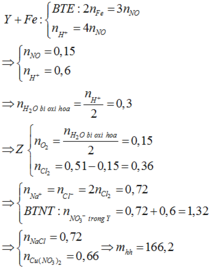

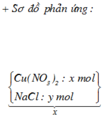
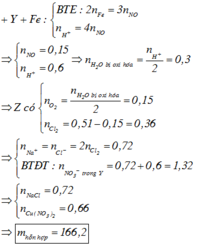

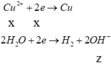
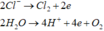
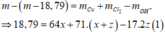
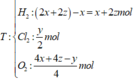
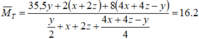
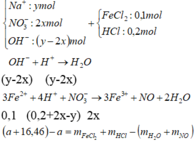
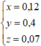
Chọn D.
Đặt số mol NaCl ban đầu lần lượt là x mol.
Khí thoát ra tại catot gồm Cl2 (0,5x mol) và O2 (0,51 – 0,5x mol)
Dung dịch Y lúc này chứa HNO3 và NaNO3.
Cho Y tác dụng tối đa với Fe (Fe lên Fe2+)