Nung m gam hỗn hợp X gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi thu được chất rắn Y. Cho Y vào H2O dư thu được 0,2m gam chất rắn Z và dung dịch E. Nhỏ từ từ dung dịch HCl 1M vào E, khi khí bắt đầu thoát ra cần dùng V1 lít dung dịch HCl và khi khí thoát ra vừa hết thì thể tích dung dịch HCl đã dùng là V2 lít. Tỉ lệ V1 : V2 tương ứng là
A. 1:3.
B. 5:6.
C.3:4.
D.1:2.

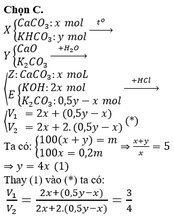

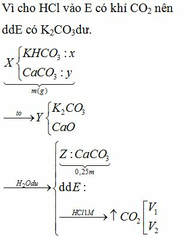
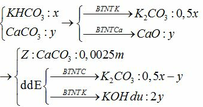
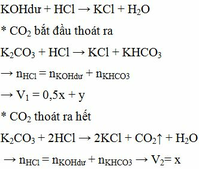
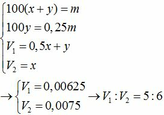
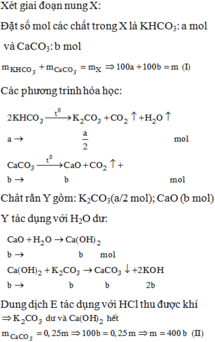

Đáp án C