Cho 10g hỗn hợp X gồm FeO, Fe2O3, S, FeS2, CuS (trong đó Oxi chiếm 16% về khối lượng) tác dụng vừa đủ với 0,335 mol H2SO4 đặc nóng sinh ra 0,2125 mol khí SO2 và dung dịch Y. Nhúng thanh Mg vào dung dịch Y, sau khi các phản ứng xảy ra hoàn toàn thì lấy thanh Mg ra thấy tăng 2,8g (giả sử 100% kim loại sinh ra bám vào thanh Mg). Đốt cháy hoàn toàn 10g X (sản phẩm gồm Fe2O3, CuO, SO2) bằng lượng vừa đủ V lit (dktc) hỗn hợp A gồm O2 và O3 tỉ lệ mol 1: 1. Giá trị của V là:
A. 1,568
B. 1,5232
C. 1,4784
D. 1,4336

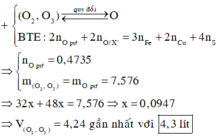

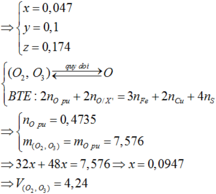
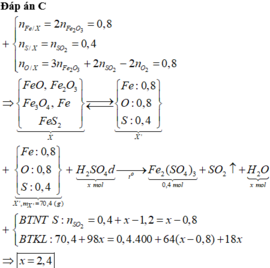
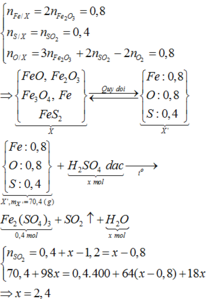
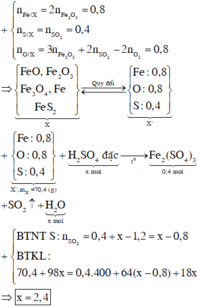

Đáp án C
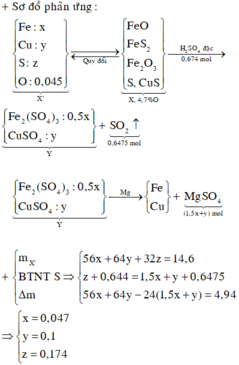
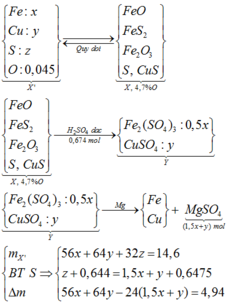
Qui đổi hỗn hợp X thành: Fe(a mol) ; Cu(b mol) ; S(c mol) ; O (0,1 mol)
(Vì oxi chiếm 16% về khối lượng => mO = 10.16% = 1,6g => nO = 1,6: 16 = 0,1 mol)
mX = 56a + 64b + 32c + 0,1.16 = 10 (1)
Trong Y có Fe3+ (a mol) ; Cu2+ (b mol) ; SO42-.
Bảo toàn điện tích: 3nFe + 2nCu = 2nSO4 => nSO4 = ½ (3a + 2b)
Bảo toàn S: nS + nH2SO4 = nSO2 + nSO4 muối
=> 0,335 + c = ½ (3a + 2b) + 0,2125 (2)
Cho Mg dư vào Y: Bảo toàn e: nMg pứ. 2 = 3nFe3+ + 2nCu2+ => nMg pứ = ½ (3a + 2b)
mKL tăng = mFe + mCu - mMg pứ => 56a + 64b – 24. ½ (3a + 2b) = 2,8 (3)
Từ (1,2,3) => a = 0,1 ; b = 0,02 ; c = 0,0475 mol
- Oxi hóa X bằng O (Qui O2 và O3 về thành O). Bảo toàn electron:
2nO = 3nFe + 2nCu + 2nS – 2nO(X)
=> 2nO = 3a + 2b + 4c – 2.0,1 => nO = 0,165 mol
- Đặt nO2 = nO3 = u => nO = 2nO2 + 3nO3 = 5u = 0,165 mol => u = 0,033 mol
=> nA = 2u = 0,066 mol
=> V = 1,4784 lit