Cho hỗn hợp X (gồm Na và Mg) lấy dư vào 100 gam dung dịch H2SO4 20% thì thể tích khí H2 (đktc) thoát ra là
A. 4,57 lít.
B. 49,78 lít
C. 54,35 lít.
D. 104,12 lít.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mH2SO4 = 20g và mH2O = 80g
Kim loại + H2SO4 → Muối + H2
Na + H2O → NaOH + ½ H2
⇒ nH2 = nH2SO4 + 0,5nH2O = 20/98 + 0,5.80/18 ⇒ V = 54,35 lít ⇒ Chọn C.

HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

Đáp án : C
Na và Mg dư thì Na phản ứng với H2O.
,nH2SO4 = 0,204 mol ; nH2O = 4,44 mol
=> nH2 = ½ (2nH2SO4 + nH2O) => VH2 = 54,35 lit

Đáp án : C
nH2SO4 = 0,204 mol ; nH2O = 4,44 mol
=> nH2 = nH2SO4 + 0,5nH2 = 2,426 mol
=> VH2 = 54,35 lit

Đáp án B
Phần chất rắn chưa tan là Al còn dư
Gọi n K = x mol
Cho hỗn hợp X vào nước, K phản ứng hết tạo KOH và Al phản ứng với KOH và còn dư => tính số mol theo KOH
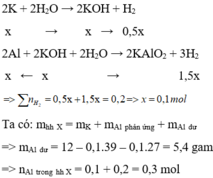
Cho hỗn hợp X tác dụng với dung dịch KOH dư => K phản ứng hết với H 2 O và Al phản ứng hết với KOH
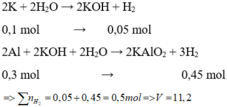
Chọn C
mH2SO4 = 20g và mH2O = 80g
Kim loại + H2SO4 → Muối + H2
Na + H2O → NaOH + ½ H2
⇒ nH2 = nH2SO4 + 0,5nH2O = 20/98 + 0,5.80/18 ⇒ V = 54,35 lít