Khi đun nóng 25,8 gam hỗn hợp ancol etylic và axit axetic có H2SO4 đặc làm xúc tác thu được 14,08 gam este. Nếu đốt cháy hoàn toàn lượng hỗn hợp ban đầu đó thu được 23,4 ml nước. Hiệu suất của phản ứng este hóa là:
A. 70%.
B. 75%.
C. 80%.
D. 85%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đ á p á n D m h h = 60 n C H 3 C O O H + 46 n C 2 H 5 O H = 25 , 8 1 B T N T H : 4 n C H 3 C O O H + 6 n C 2 H 5 O H = 2 n H 2 O = 2 , 6 2 1 , 2 ⇒ n C 2 H 5 O H = 0 , 2 n C H 3 C O O H = 0 , 3 H = 14 , 08 0 , 2 . 88 . 100 % = 80 %

Chọn đáp án B
25,8 gam gồm x mol C2H5OH và y mol CH3COOH đốt thu được 1,3 mol H2O.
Giải hệ tìm x = 0,3 mol và y = 0,2 mol.
Este là CH3COOC2H5
→ 14,08 gam ⇄ 0,16 mol.
Phản ứng este hóa:
C H 3 C O O H + C 2 H 5 O H → C H 3 C O O C 2 H 5 + H 2 O
Từ các số liệu trên và tỉ lệ phản ứng
→ H được tính theo axit là chất "ít dư" hơn
→ Yêu cầu:
H% = 0,16 ÷ 0,2 = 80%

Giải thích:
n H2O = 23,4 : 18 = 1,3 mol ( 1ml = 1g đối với nước )
Đặt số mol của CH3COOH là a , số mol của C2H5OH là b ta có hệ
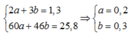
n este = 14,08 : 88 = 0,16 mol
CH3COOH + C2H5OH→ CH3COOC2H5 + H2O
0,2 0,3 => 0,2 mol ( theo lý thuyết )
![]()
Đáp án D

Đáp án: D
Gọi nCH3COOH = x ; nC2H5OH = y
=> 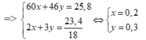
=> % CH3COOH = = 46,5% ; % C2H5OH = 53,5%
Gọi hiệu suất phản ứng este hóa là H.
=> n este = 0,2.H (vì axit hết - theo lí thuyết)
=> meste = 0,2H.88 = 17,6H
Mà meste = 14,08
=> H = 80%

Gọi n C 2 H 5 O H = x ; n C H 3 C O O H = y . Đốt cháy sản phẩm cũng như hỗn hợp ban đầu, theo định luật bảo toàn nguyên tố H ta có:
6 n C 2 H 5 O H + 4 n C H 3 C O O H = 2 n H 2 O
Hay 6x + 4y = 2. 23 , 4 18 = 2,6 (1)
Phương trình theo khối lượng: 46x + 60y = 25,8 (2)
Từ (1) và (2) suy ra: x = 0,3; y = 0,2
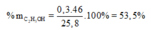
![]()
Theo lý thuyết n e s t e = n a x i t = 0 , 2
⇒ m e s t e = 17 , 6 ( g ) mà thực tế thu được 14,08 (g)
Vậy H = 14 , 08 17 , 6 . 100 % = 80 %
Đáp án D

Chọn đáp án D
Đặt nC2H5OH = x; nCH3COOH = y
⇒ 46x + 60y = 25,8(g).
Lại có:
DH2O = 1g/ml
⇒ nH2O = 23,4 × 1 ÷ 18 = 1,3 = 3x + 2y
⇒ Giải hệ có:
x = 0,3 mol; y = 0,2 mol
⇒ hiệu suất tính theo CH3COOH.
nCH3COOC2H5 = 14,08 ÷ 88 = 0,16 mol
⇒ H = 0,16 ÷ 0,2 × 100% = 80%.
Chọn C.