Khối lượng P2O5 có trong 5 tấn quặng photphat chứa 35% Ca3(PO4)2 là
A. 0,5 tấn B. 0,8 tấn C. 0,7 tấn D. 0,85 tấn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{Ca_3\left(PO_4\right)_2}=20\cdot40\%=8\left(tấn\right)=8000\left(kg\right)\)
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{8000}{310}=\dfrac{800}{31}\left(kmol\right)\)
Bảo toàn nguyên tố P :
\(n_{P_2O_5}=n_{Ca_3\left(PO_4\right)_2}=\dfrac{800}{31}\left(kmol\right)\)
\(m_{P_2O_5}=\dfrac{800}{31}\cdot142=3664.5\left(kg\right)\)

Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P ⇒ trong 1 mol Ca3(PO4)2 có 1mol P2O5 nghĩa là trong 310g Ca3(PO4)2 tương ứng có 142g P2O5.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
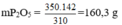
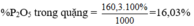

Quặng hemantit chứa thành phần chính là : Fe2O3
Bảo toàn nguyên tố Fe: \(n_{Fe_2O_3}.2=n_{Fe}\\ \Rightarrow n_{Fe_2O_3}=0,0225\left(mol\right)\\ VìH=80\%\Rightarrow m_{Fe_2O_3}=\dfrac{0,0225}{80\%}.160=4,5\left(tấn\right)\\ m_{quặng}=\dfrac{4,5}{82\%}=5,488\left(tấn\right)\)

Gọi khối lượng của quặng loại I là x(tấn)
(Điều kiện: 0<x<=10)
Khối lượng của quặng loại II là 10-x(tấn)
Tỉ lệ sắt nguyên chất trong quặng loại I là \(\dfrac{0.8}{x}\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại II là \(\dfrac{0.6}{10-x}\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%=0,1 nên ta có;
\(\dfrac{0.8}{x}-\dfrac{0.6}{10-x}=0.1\)
=>\(\dfrac{8}{x}-\dfrac{6}{10-x}=1\)
=>\(\dfrac{8}{x}+\dfrac{6}{x-10}=1\)
=>\(\dfrac{8x-80+6x}{x\left(x-10\right)}=1\)
=>\(x\left(x-10\right)=14x-80\)
=>\(x^2-24x+80=0\)
=>(x-20)(x-4)=0
=>\(\left[{}\begin{matrix}x-20=0\\x-4=0\end{matrix}\right.\)
=>\(\left[{}\begin{matrix}x=20\left(loại\right)\\x=4\left(nhận\right)\end{matrix}\right.\)
Vậy: Khối lượng quặng loại I là 4 tấn
Khối lượng quặng loại II là 10-4=6 tấn

Gọi khối lượng quặng loại 1 là x ( \(x\ne0\) )
Khối lượng quặng 2 là : \(10-x\left(tấn\right)\)
Tỉ lệ sắt nguyên chất trong quặng loại I là: \(\dfrac{0,8}{x}\)
Tỉ lệ sắt nguyên chất trong quặng loại II là: \(\dfrac{0,6}{10-x}\)
Do tỉ lệ sắt nguyên chất trong quặng loại I nhiều hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%
Nên ta có phương trình:
\(\dfrac{0,8}{x}-\dfrac{0,6}{10-x}=\dfrac{10}{100}\)
\(\Leftrightarrow0,8\left(10-x\right)-0,6x=0,1x\left(10-x\right)\)
\(\Leftrightarrow8\left(10-x\right)-6x=x\left(10-x\right)\)
\(\Leftrightarrow80-8x-6x=10x-x^2\)
\(\Leftrightarrow x^2-24x+80=0\)
\(\Leftrightarrow x\left(x-20\right)-4\left(x-20\right)=0\)
\(\Leftrightarrow\left(x-20\right).\left(x-4\right)=0\)
\(\Leftrightarrow\left[{}\begin{matrix}x-20=0\\x-4=0\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}x=20\left(l\right)\\x=4\left(n\right)\end{matrix}\right.\)
Vậy: Khối lượng quặng loại I là 4 tấn, khối lượng quặng loại I là: 10 – 4 = 6 tấn.
Giúp câu này vứi ạk
Có hai loại quặng sắt, quặng loại 1 và loại II, tổng khối lượng là 12 tấn khối sắt nguyên chất trong quặng loại I là 1,8 tấn, trong quặng loại II là 1,6 tấn. Biết tỉ lệ sắt nguyên chất trong quặng loại 1 hơn tỉ lệ sắt nguyên chất trong quặng loại II là 10%. Tính khối lượng mỗi loại quặng.
\(m_{Ca_3\left(PO_4\right)_2}=5.35\%=1,75\left(tấn\right)\)
Trong 1 mol Ca3(PO4)2 có 1 mol P2O5
=> Trong 310 tấn Ca3(PO4)2 tương ứng có 142 tấn P2O5
=> Trong 1,75 tấn Ca3(PO4)2 tương ứng có x tấn P2O5
=> x=\(\dfrac{1,75.142}{310}=0,8\left(tấn\right)\)
=> Chọn B