Cho H2 và 1 olefin có thể tích bằng nhau qua Ni đun nóng ta được hỗn hợp A . Biết tỉ khối hơi của A đối với H2 là 23,2. Hiệu suất phản ứng hiđro hoá là 75%. Công thức phân tử olefin là
A. C2H4
B. C3H6
C. C4H8
D. C5H10
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Hướng dẫn Giả sử nanken = nH2 = 1 mol; nA = 2- 0,75 = 1,25 mol
Mđ = 23,2.2.1,25/2 = 14,5; 14.n + 2 = 2.14,5 => n = 4

Giả sử nH2 = nX = 1
nA = n hỗn hợp – nH2 phản ứng = 2 – 0,75 = 1,25
m hỗn hợp = mA ⇒ 2 + MX = MA.1,25 = 23,2.1,25 .2
⇒ MX = 56
⇒ X là C4H8.
Đáp án C.

Đáp án C
Hướng dẫn dẫn
Theo giả thiết ta chọn : n H 2 = n C n H 2 n = 1 mol
Phương trình phản ứng :
CnH2n + H2 → N i , t 0 CnH2n+2 (1)
Theo (1) ta thấy, sau phản ứng số mol khí giảm một lượng đúng bằng số mol H2 phản ứng. Hiệu suất phản ứng là 75% nên số mol H2 phản ứng là 0,75 mol. Như vậy sau phản ứng tổng số mol khí là 1+1 – 0,75 = 1,25 mol
Áp dụng định luật bảo toàn khối lượng ta có : khối lượng của H2 và CnH2n ban đầu bằng khối lượng của hỗn hợp A
M - A = 1 . 2 + 1 . 14 n 1 , 25 = 23,2.2 => n = 4
Vậy công thức phân tử olefin là C4H8

Đáp án C
Giả sử số mol H2 và olefin đều là 1 mol
Ta có: ![]()
![]()
Vậy olefin đó là C4H8.

Đáp án D
hhX gồm H2 và CnH2n có tỉ lệ số mol là 1 : 1.
hhX qua ống đựng Ni, to → hhY có dY/H2 = 23,2. H = b%.
• Coi hh X gồm H2 1 mol; CnH2n - 2 1 mol.
hhY gồm CnH2n + 2 x mol; H2 dư (1 - x) mol và CnH2n (1 - x) mol.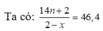
→ 14n + 46,4x = 90,8.
Biện luận → n = 4; x = 0,75 → C4H7; H = 75%

Đáp án A
![]()
![]()
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
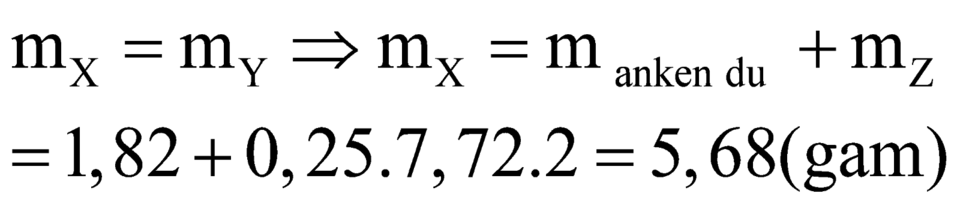
Mà ![]()
![]()
![]()
Do đó hai anken trong X là C2H4 và C3H6.
Cách 1: Áp dụng sơ đồ đường chéo hoặc giải hệ phương trình, ta có:
![]()
Cách 2: Ta có: ![]()
![]()
Vì ![]() nên
nên ![]()

Đáp án A
Vì nH2phản ứng = nanken phản ứng = nankan
→ nZ = nH2dư + nankan = nH2ban đầu = 0,25 mol.
→ nanken ban đầu = 0,4 - 0,25 = 0,15 mol.
Gọi x = nCnH2n + 2 → nH2dư = 0,25 - x (mol)
→ mZ = (14n + 2)x + 2(0,25 - x) = 0,25 x 7,72 x 2
→ 14nx = 3,36 (1)
nCnH2ndư = 0,15 - x → 14n(0,15 - x) = 1,82 (2)
Từ (1), (2) → x = 0,01; n = 2,47
→ C2H4 và C3H6.
• Đặt nC2H4 = a mol; nC3H6 = b mol.
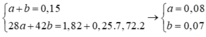
![]()
Gọi CT của olefin là CnH2n có số mol là x
+/ CnH2n + H2 → CnH2n+2
Ban đầu x x
Phản ứng 0,75x 0,75x
Cân bằng 0,25x 0,25x 0,75x
=> n A = 1,25x mol
=>m A = 2.23,2 . 1,25x = m hỗn hợp đầu = 14nx + 2x
=>n= 4 => Olefin là C4H8
=>C