Lấy cùng một lượng K C l O 3 và K M n O 4 để điều chế oxi. Chất nào tạo ra nhiều khí O 2 hơn. Nếu điều chế dùng một thể tích khí oxi thì dùng chất nào kinh tế hơn? Biết rằng giá K M n O 4 là 30.000 đ/kg và K C l O 3 là 96.000 đ/kg.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử ta lấy cùng một khối lượng là a g
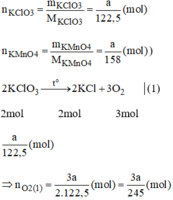
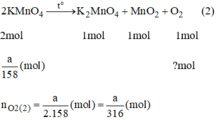
Vậy 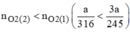 nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3

a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.

Gọi m KClO3 và m KMnO4=a
-->n KClO3=a/122,4
n KMnO4=a/158(mol)
2KClO3--->2KCl+3O2
a/122,5------------>a/81,667(mol)
2KMnO4---->K2MnO4+MnO2+O2
a/158--------------------------------a/316(mol)
\(\frac{a}{81,667}>\frac{a}{316}\)
-->KClO3 cho nhiều khí hơn
b)

- giả sử lấy 1 mol KClO3 và 1 mol KMnO4
PTHH: 2 KClO3 -to-> 2 KCl + 3 O2
1_________________1_______1,5(mol)
2 KMnO4 -to-> K2MnO4 + MnO2 + O2
1____________0,5__________0,5__0,5(mol)
Vì 1,5 > 0,5 => Nếu cùng 1 lượng KClO3 và KMnO4 thì lượng O2 điều chết từ KClO3 sẽ nhiều hơn.
b)
PTHH: 2 KClO3 -to-> 2 KCl + 3 O2
2/3_________________2/3_______1(mol)
2 KMnO4 -to-> K2MnO4 + MnO2 + O2
2____________1__________1__1(mol)
Ví dụ cùng 1 mol O2.
Ta có , số tiền mua KMnO4= 30 000 . (316/1000)=9480 (đồng)
số tiền mua KClO3= 96000.((245/3) /1000)= 7840(đồng)
Vì 9480>7840 nên nếu cùng 1 thể tích O2 thì dùng KMnO4 kinh tế hơn.

sao chị ko đáp lại câu trả lời của em ở câu trước , chị ko biết hả ?

b>
Giả sử mỗi chất đều có khối lượng là 1 gam
nKMnO4=0,00633mol
nKClO3=0,00816mol
nMnO2=0,0115mol
nK2Cr2O7=0,0034mol
Các phản ứng :
2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,00663 --------------------------- →0,0158
KClO3 + 6HCl -> KCl + 3Cl2 + 3H2O
0,00816 -------------- → 0,0245
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
0,0115------------------- → 0,0115
K2Cr2O7 + 14HCl -> 2KCl + 2CrCl3 + 3Cl2 + 7H2O
0,0034 ---------------------------------- →0,0102
=> Chất cho lượng khí lớn nhất là Cl2 : KClO3.

Theo bài ra : KMnO4 và KClO3 có cùng khối lượng x (g)
Suy ra : nKMnO4 = \(\dfrac{x}{158}\) (mol)
nKClO3 = \(\dfrac{x}{122,8}\) (mol)
PTHH có : 2KMnO4 \(\rightarrow\) K2MnO4 + MnO2 + O2
(mol) \(\dfrac{x}{158}\) \(\dfrac{x}{316}\)
2KClO3 \(\rightarrow\) 2KCl + 3O2
(mol) \(\dfrac{x}{122,8}\) \(\dfrac{3x}{245,8}\)
Ta có: \(\dfrac{x}{136}< \dfrac{3x}{245,8}\) (mol)
Vậy Nếu lấy KClO3 và KMnO4 cùng khối lượng thì KClO3 điều chế đc nhiều oxi hơn.

* Ta có PTHH:
2KMnO4 \(\rightarrow\) K2MnO4 + MnO2 + O2 (1)
2KClO3 \(\rightarrow\) 2KCl + 3O2 (2)
Gọi mKMnO4 = mKClO3 =a (g)
=> nKMnO4 = a/158 (mol) và nKClO3 = a/122.5 (mol)
Theo PT (1) => nO2 = 1/2 . nKMnO4 = 1/2 . a/158 = a/316 (mol)
Theo PT(2) => nO2 = 3/2 . nKClO3 = 3/2 . a/122.5 = 3/245 .a (mol)
Có : 1/316 < 3/245 => a/316 < 3/245 .a
hay nO2(PT1) < nO2(PT2)
=> KClO3 cho nhiều khí O2 hơn
TheO PT(2)

gọi a là khối lương 2 chất
2KMnO4 -to> MnO2+ O2+ K2MnO4
nKMnO4=\(\dfrac{a}{142}\)->n O2=\(\dfrac{a}{245}\)
2KClO3-to> 3O2+2KCl
nKClO3=\(\dfrac{a}{122,5}\)->n O2=\(\dfrac{a}{\dfrac{611}{3}}\)
ta sa sánh : \(\dfrac{a}{245}\)<\(\dfrac{a}{\dfrac{611}{3}}\)
=> KClO3 cho nhiều O2 hơn
giả sử số gam của 2 chất là a
=> mKMnO4 = a/158 , mKClO3 = a/122,5
pthh : 2KMnO4 -t--> K2MnO4 +MnO2 + O2
a/158 -----------------------------------> a/316(mol)
2KClO3 -t---> 2KCl + 3O2
a/122,5---------------->3a/245(mol)
so sánh a/316 < 3a/245
=> KClO3 sinh ra có thể tích Oxi lớn hơn KMnO4


Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.