Trong ion âm X3- có tổng số các hạt là 111 hạt trong đó số hạt electron bằng 48% số khối. Số nơtron của X là
A. 75
B. 33
C. 36
D. 42
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Theo giả thiết ta có: 2 Z X + 2 Z Y + N X + N Y = 142 ( 2 Z X + 2 Z Y ) - ( N X + N Y ) = 42 ⇔ Z X + Z Y = 46 ( 1 ) N X + N Y = 50 ( 2 )
Mặt khác ta lại có: Tỉ lệ số proton của ion X 2 + và ion Y 3 + là 10 13 ⇒ Z X Z Y = 10 13 ( 3 )
Từ (1) và (3) ta có Z X = 20 ( C a ) v à Z Y = 26 ( F e )
X có cấu hình electron là: 1s22s22p63s23p64s2.
⇒ X có 0 electron độc thân
Fe có cấu hình là 1s22s22p63s23p63d64s2
⇒ F e 3 + có cấu hình là 1s22s22p63s23p63d5
⇒ F e 3 + có 5 electron độc thân
Chú ý: Đây là một bài khá dễ nhưng sẽ có nhiều bạn mắc phải sai lầm đáng tiếc là khi đề cho giả thiết: Tỉ lệ số proton của ion X 2 + và ion Y 3 + là 10 13
Theo quán tính sẽ có rất nhiều bạn sẽ thành lập phương trình sau: Z X - 2 Z Y - 3 = 10 13 dẫn đến không tìm ra kết quả đúng. Ở đây giả thiết cho là proton (hạt mang điện trong hạt nhân) chứ không phải electron (hạt mang điện lớp vỏ). Vì vậy trong quá trình làm bài các bạn nên đọc thật kỹ đề và không nên làm theo quán tính đọc hiểu đề và tư duy ngay cách làm.


X có cấu hình electron là: 1s22s22p63s23p64s2.
⇒ X có 0 electron độc thân
Fe có cấu hình là 1s22s22p63s23p63d64s2
⇒ F e 3 + có cấu hình là 1s22s22p63s23p63d5
⇒ F e 3 + có 5 electron độc thân
Chú ý: Đây là một bài khá dễ nhưng sẽ có nhiều bạn mắc phải sai lầm đáng tiếc là khi đề cho giả thiết: Tỉ lệ số proton của ion X 2 + và ion Y 3 + là 10 13
Theo quán tính sẽ có rất nhiều bạn sẽ thành lập phương trình sau: Z X - 2 Z y - 3 = 10 13 dẫn đến không tìm ra kết quả đúng. Ở đây giả thiết cho là proton (hạt mang điện trong hạt nhân) chứ không phải electron (hạt mang điện lớp vỏ). Vì vậy trong quá trình làm bài các bạn nên đọc thật kỹ đề và không nên làm theo quán tính đọc hiểu đề và tư duy ngay cách làm.
Đáp án C

Đáp án C.
Gọi p, e, n là số proton, số electron và số nơtron trong một nguyên tử M; p’, e’, n’ là số proton, số electron và số nơtron trong một nguyên tử X.
Trong nguyên tử số proton = số electron; các hạt mang điện là proton và electron, hạt không mang điện là nơtron.
+ Trong phân tử của M2X2 có tổng số hạt proton, nơtron và electron là 164 nên suy ra:
2(2p + n) + 2(2p’ + n’) = 164 (1)
+ Trong đó số hạt mang điện nhiều hơn hạt không mang điện là 52 nên suy ra:
(4p + 4p’) - 2(n + n’) = 52 (2)
+ Số khối của M lớn hơn số khối của X là 23 đơn vị nên ta có suy ra:
(p + n) - (p’ + n’) = 23 (3)
+ Tổng số hạt electron trong M+ nhiều hơn trong X22- là 7 hạt nên suy ra:
(2p + n - 1) - 2(2p’ + n’) + 2 = 7 (4)
Giải hệ (1), (2), (3), (4) ta được p = 19 ⇒ M là kali; p’ = 8 ⇒ X là oxi.
Công thức phân tử của hợp chất là K2O2.

Đáp án B.
Tổng số các loại hạt proton, nơtron và electron của X2+ là 92
p + n + e -2 = 92 => 2p + n = 94 (1)
Tổng số hạt mang điện gấp nhiều hơn số hạt không mang điện là 20
(p + e -2) – n = 20 hay 2p – n = 22 (2)
Từ (1), (2) ta có p = e = 29 , n =36

Đáp án A
X + 3e → X3-
Vậy ZX = 111 - 3 = 108 → 2Z + N = 108.
Ta có:
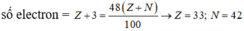
Vậy X có số khối: A = Z + N = 33 + 42 = 75

Giả sử Z, N lần lượt là số hiệu nguyên tử và số nơtron của nguyên tử X3-.
Ta có hpt:
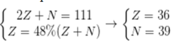
Số electron của X = 36 - 3 = 33 hạt.
Số hạt mang điện của X là 33 x 2 = 66 hạt.
Số khối của X là A = Z + N = 36 + 39 = 75
→ Chọn A.

A
X + 3e → X3-
Vậy ZX = 111 - 3 = 108 → 2Z + N = 108.
Ta có: số electron = ![]() → Z = 33; N = 42
→ Z = 33; N = 42
Vậy X có số khối: A = Z + N = 33 + 42 = 75 → Chọn A
Chọn D