Cho 9,6 gam hỗn hợp X gồm Mg và Fe3O4 vào 300 ml dung dịch HNO3 2M thu được dung dịch Y và 0,896 lít (đktc) hỗn hợp khí gồm N2O và NO có tỉ khối so với H2 bằng 16,75. Trung hòa dung dịch Y cần dùng 40 ml dung dịch NaOH 1M thu được dung dịch A. Khối lượng chất tan trong dung dịch A bằng:
A. 42,26 gam.
B. 19,76 gam.
C. 28,46 gam.
D. 72,45 gam.


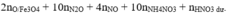

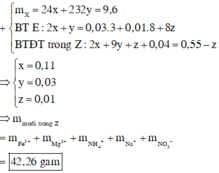
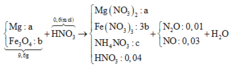


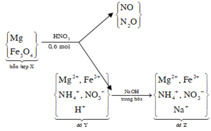



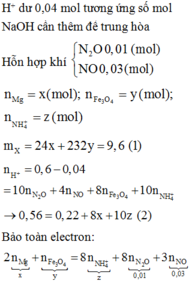
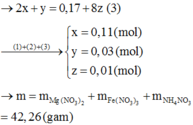
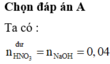
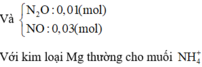
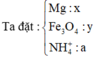
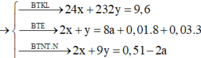
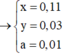
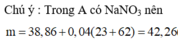
Chọn đáp án A
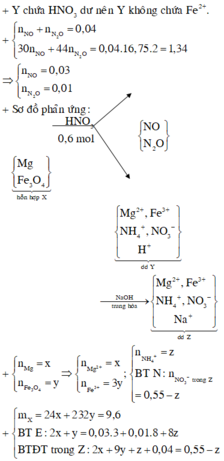
Đặt nN2O = x; nNO = y ⇒ nkhí = x + y = 0,04 mol; mkhí = 44x + 30y = 0,04 × 16,75 × 2.
Giải hệ có: x = 0,01 mol; y = 0,03 mol || nH+ dư = nNaOH = 0,04 mol.
Đặt nMg = x; nFe3O4 = y; nNH4NO3 = z ⇒ mX = 24x + 232y = 9,6(g). Bảo toàn electron:
2x + y = 8z + 0,01 × 8 + 0,03 × 3 || Lại có: nH+ phản ứng = 2nO + 10nNH4+ + 10nN2O + 4nNO
⇒ 0,6 - 0,04 = 2 × 4y + 10z + 10 × 0,01 + 4 × 0,03 ||⇒ giải hệ có:
x = 0,11 mol; y = 0,03 mol; z = 0,01 mol. A gồm Mg(NO3)2, Fe(NO3)3, NH4NO3, NaNO3.
► mchất tan = 0,11 × 148 + 0,09 × 242 + 0,01 × 80 + 0,04 × 85 = 42,26(g) ⇒ chọn A