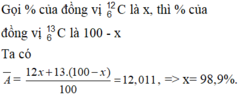Trong tự nhiên cacbon có 2 đồng vị bền 12 6 C và 13 6 C . Nguyên tử khối trung bình của nguyên tố cacbon là 12,011. - Tính thành phần phần trăm số nguyên tử của mỗi đồng vị cacbon. - Tính thành phần phần trăm khối lượng của 12C có trong C2H6 (với H là đồng vị 1 1H )
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x,y lần lượt là phần trăm đồng vị của 12C và 13C
Ta có: \(\left\{{}\begin{matrix}x+y=100\\12.0,01x+13.0,01y=12,011\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=100-y\\0,12.\left(100-y\right)+0,13.y=12,011\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=98,9\%\\y=1,1\%\end{matrix}\right.\)

Chọn A
Gọi % số nguyên tử của đồng vị C 6 13 là x %, thì % số nguyên tử của đồng vị C là 100 – x (%).
Ta có
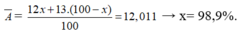

Chọn A
Gọi % của đồng vị 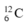 là x, thì % của đồng vị
là x, thì % của đồng vị 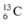 là 100 - x
là 100 - x
Ta có
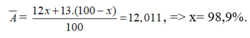 .
.

Nguyên tử khối trung bình của nguyên tố cacbon là :
M = \(\frac{12.98,89+13.1,11}{100}=12,011\)
→ Chọn B

a) Đặt %24Mg là x
-->%25Mg là (100 - x - 11)
\(\overline{M}=\dfrac{x.24+\left(100-x-11\right).25+11.26}{100}=24,32\)
\(\Rightarrow x=\%^{24}Mg=79\%\)
b) ta có : \(n_{Mg}=n_{MgCl2}=1\left(mol\right)\Rightarrow n_{26_{Mg}}=1.11\%=0,11\left(mol\right)\)
Số nguyên tử : \(0,11.6,022.10^{-3}=6,6022.10^{-4}\)(nguyên tử)