Cho 14,4 gam hỗn hợp Fe, Mg và Cu (số mol mỗi kim loại bằng nhau) tác dụng hết với dung dịch HNO3 (dư), thu được dung dịch X và 2,688 lít (đktc) hỗn hợp gồm 4 khí N2, N2O, NO và NO2 trong đó hai khí N2 và NO2 có số mol bằng nhau. Cô cạn cẩn thận toàn bộ X thu được 58,8 gam muối khan. Số mol HNO3 đã tham gia phản ứng là
A. 0,725.
B. 0,923.
C. 0,945.
D. 0,893.


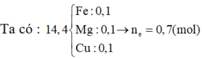
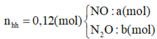
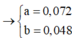
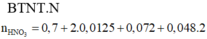

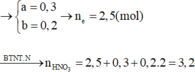


gt ⇒ nFe = nMg = nCu = 0,1 mol
N2 = nNO2 ⇒ ghép: N2 + NO2 = N3O2 = N2O.NO = N2O + NO.
► Quy hỗn hợp khí về N2O và NO với số mol x và y
nkhí = x + y = 0,12 mol. HNO3 dư ⇒ Fe lên +3.
● mFe(NO3)3 + mMg(NO3)2 + mCu(NO3)2 = 0,1 × 242 + 0,1 × 148 + 0,1 × 188 = 57,8(g) < 58,8(g).
⇒ chứa muối NH4NO3 ⇒ nNH4NO3 = (58,8 - 57,8) ÷ 80 = 0,0125 mol. Bảo toàn electron:
3nFe + 2nMg + 2nCu = 8nN2O + 3nNO + 8NH4NO3 ⇒ 8x + 3y = 0,6 mol
⇒ x = 0,048 mol; y = 0,072 mol.
► nHNO3 = 10nN2O + 4nNO + 10nNH4NO3 = 0,893 mol
Đáp án D