Nung nóng 19,15 gam hỗn hợp CuO và PbO với một lượng cacbon vừa đủ trong môi trường không có oxi để oxit kim loại bị khử hết. Toàn bộ lượng khí sinh ra được dẫn vào dung dịch Ca OH 2 dư, phản ứng xong người ta thu được 7,5 gam chất kết tủa màu trắng. Viết phương trình hoá học của các phản ứng đã xảy ra
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có các phương trình: 80x + 223y = 19,15 (I)
x/2 + y/2 = 0,075 (l)
Giải phương trình (I), (II), ta được: X =0,1 ; Y=0,05
m CuO = 8g; m PbO = 11,15g
Vậy CuO chiếm 8/19,15 x 100% = 41% khối lượng hỗn hợp đầu, còn PbO chiếm: 59%

a) \(2CuO+C-^{t^o}\rightarrow2Cu+CO_2\)
\(2PbO+C-^{t^o}\rightarrow2Pb+CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
b) \(n_C=0,075\left(mol\right);n_{CO_2}=0,06\left(mol\right)\)
Vì nCO2 < nC => Sau phản ứng C dư
Gọi x,y là số mol của CuO, PbO
Ta có : \(\left\{{}\begin{matrix}\dfrac{1}{2}x+\dfrac{1}{2}y=0,06\\80x+223y=12,46\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,02\end{matrix}\right.\)
=> \(\%m_{CuO}=\dfrac{0,1.8}{12,46}.100=64,21\%\)
%m PbO =35,79%

_Nung nóng hỗn hợp gồm CuO và PbO bằng C:
Gọi a,b là số mol của CuO và PbO:
=>80a+223b=19.15(1)
2CuO+C(t*)=>2Cu+CO2
a------->0.5a--->a--->0.5a(mol)
2PbO+C(t*)=>2Pb+CO2
b------>0.5b---->b---->0.5b(mol)
_Cho CO2 sản phẩm vào dd Ca(OH)2 thu được kết tủa trắng CaCO3:
+nCaCO3=7.5/100=0.075(mol)
CO2+Ca(OH)2=>CaCO3+H2O
0.075---------------->0.075(mol)
=>0.5a+0.5b=0.075(2)
Từ(1)(2)=>a=0.1,b=0.05
=>mCuO=0.1*80=8(g)
=>mPbO=0.05*223=11.15(g)
+nCu=0.1(mol)
=>mCu=0.1*64=6.4(g)
+nPb=0.05(mol)
=>mPb=0.05*207=10.35(g)
=>m(KL)=6.4+10.35=16.75(g)
c)
+nC=0.5(a+b)=0.5(0.1+0.05)=0.075(mol)
=>mC=0.075*12=0.9(g)

Gọi $n_{CuO} = a; n_{PbO} = b$
Ta có :
$80a + 223b = 15,15(1)$
$CuO + CO \xrightarrow{t^o} Cu + CO_2$
$PbO + CO \xrightarrow{t^o} Pb + CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Theo PTHH :
$n_{CO_2} = a + b = \dfrac{10}{100} = 0,1(2)$
Từ (1)(2) suy ra a = b = 0,05
Vậy :
$m_{CuO} = 0,05.80 = 4(gam)$
$m_{PbO} = 0,05.223 = 11,15(gam)$

a,\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(n_{CaCO3}=n_{CO2}=0,075\left(mol\right)\)
\(2CuO+C\underrightarrow{^{to}}Cu+CO_2\)
a______0,5a__a_____0,5a
\(2PbO+C\underrightarrow{^{to}}Pb+CO_2\)
b_____0,5b___b___0,5b
Giải hệ PT:
\(\left\{{}\begin{matrix}80a+233b=19,15\\0,5a+0,5b=0,075\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\)
\(\%_{CuO}=\frac{0,1.80.100}{19,15}=41,78\%\)
\(\%_{PbO}=100\%-41,78\%=58,22\%\)
\(m_{Cu}=64a=6,4\left(g\right)\)
\(m_{Pb}=207b=10,35\left(g\right)\)
b, \(n_C=0,5.\left(a+b\right)=0,075\left(mol\right)\)
\(\Rightarrow m_C=0,9\left(g\right)\)
a) - nCuO = x ; nPbO= y
=> mhh = 80x +223y=19.15 (1)
- Bảo toàn C : nCO2 = nCaCO3 =0.075
- Bảo toàn O => x+y = 2 nCO2 = 0.15 (2)
- (1) + (2) => x=0.1 , y= 0.05
=> %mCuO = 41.78% ; %mPbO = 58.22%
- mCu = 6.4 g ; mPb= 10.35
b) - nC= nCO2 = 0.075
=> mC= 0.9g
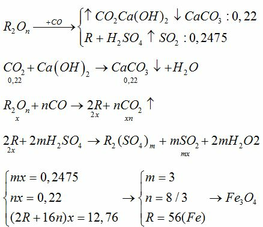
Phương trình hóa học:
2CuO + C → 2Cu + CO 2
2PbO + C → 2Pb + CO 2
CO 2 + Ca OH 2 → CaCO 3 + H 2 O
n CaCO 3 = 7,5/100 = 0,075
n C u O = x; n P b O = y