Dãy gồm nguyên tử X và các ion Y 2 + , Z - đều có cấu hình electron phân lớp ngoài cùng 3 p 6 là:
![]()
![]()
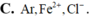
![]()
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án D
Cấu hình electron của nguyên tử X là 1s22s22p63s23p6
Số thứ tự của X = số electron = 18 → X là Ar.
• Y → Y2+ + 2e
Cấu hình electron của Y là 1s22s22p63s23p64s2
Số thứ tự của Y = số electron = 20 → Y là Ca2+.
• Z + 1e → Z-
Cấu hình electron của Z là 1s22s22p63s23p5
Số thứ tự của Z = số electron = 17 → Z là Cl.
→ Chọn D.

Đáp án C
- X+: 1s22s22p6 → X: 1s22s22p63s1 → X là Na
- Y-: 1s22s22p6 → Y: 1s22s22p5 → Y là F
- Z: 1s22s22p6 → Z là Ne

Sửa đề 1 chút nhé bạn :
Tổng số e ở phân lớp ngoài cùng của X và Y là 7
Nếu là 6 thì e ngoài cũng của tất cả các trường hợp điều thỏa mãn mất rồi!
TH1: Y có phân lớp ngoài cùng là 3s1
→ Y có cấu hình electron là 1s22s22p63s1
→ Y có 11e → Y có Z = 11.
X có số electron ở phân lớp ngoài cùng = 7 - 1 = 6
→ X có phân lớp ngoài cùng là 3p6 → X là khí hiếm → loại.
• TH2: Y có phân lớp ngoài cùng là 3s2 → tương tự ta có Y có Z = 12.
Khi đó, X có lớp ngoài cùng là 3p5
→ X có cấu hình electron là 1s22s22p63s23p5
→ X có 17 e → Z = 17.