Đốt cháy hết hỗn hợp gồm metan và axetilen có thể tích 5,6 lít (đktc), cho sản phẩm quan một lượng dư dung dịch C a ( O H ) 2 thu được 40 g C a C O 3 . Thành phần % theo thể tích của axetilen trong hỗn hợp ban đầu là
A. 60%
B. 50%
C. 40%
D. 30%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

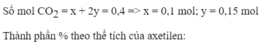
![]()

\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{80}{100}=0,8mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,8 0,8 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,5\\x+2y=0,8\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,5}.100=40\%\)
\(\%V_{C_2H_2}=100\%-40\%=60\%\)
Gọi a (mol) và b (mol) lần lượt là số mol của khí metan (CH4) và khí axetilen (C2H2).
Giả thiết: a+b=11,2/22,4=0,5 (1).
Số mol kết tủa CaCO3 là 80/100=0,8 (mol) bằng số mol sản phẩm khí CO2 (do dung dịch Ca(OH)2 dư).
Ta có: a+2b=0,8 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,2 (mol) và b=0,3 (mol).
Thành phần phần trăm thể tích mỗi chất khí trong hỗn hợp ban đầu:
%Vmetan=0,2/0,5.100%=40%, suy ra %Vaxetilen=100%-40%=60%.

mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> \(n_{CH_4}=\dfrac{8,96}{22,4}-0,2=0,2\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,2--->0,4
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,2---->0,6
=> VO2 = (0,4 + 0,6).22,4 = 22,4 (l)
=> Vkk = 22,4.5 = 112 (l)

\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_4:y\left(mol\right)\end{matrix}\right.\)⇒ x + y = \(\dfrac{8,96}{22,4} = 0,4\)(1)
\(m_{CO_2} + m_{H_2O} = m_{bình\ tăng} = 45,2(gam)\)
Bảo toàn nguyên tố với C:\(n_{CO_2} = x + 2y(mol)\)
Bảo toàn nguyên tố với H:\(n_{H_2O} = 2x + 2y (mol)\)
Suy ra :(x + 2y).44 + (2x+2y).18 = 45,2(2)
Từ (1)(2) suy ra: x = 0,1 ; y = 0,3
Vậy :
\(\%V_{CH_4} = \dfrac{0,1}{0,4}.100\% = 25\%\\ \%V_{C_2H_4} = 100\% - 25\% = 75\%\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CaCO_3} = n_{CO_2} = 0,1 + 0,3.2 = 0,7(mol)\\ \Rightarrow m = 0,7.100 = 70(gam)\)

\(Đặt:n_{CH_4}=a\left(mol\right),n_{C_2H_2}=b\left(mol\right)\)
\(n_{hh}=a+b=0.35\left(mol\right)\left(1\right)\)
\(BTC:\)
\(a+2b=0.6\)
\(a=1\)
\(b=0.25\)
\(\%CH_4=\dfrac{0.1}{0.35}\cdot100\%=28.57\%\)
\(\%C_2H_2=71.43\%\)
\(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)⇒ x + y = \(\dfrac{7,84}{22,4} = 0,35(mol)\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_2 + \dfrac{5}{2}O_2 \xrightarrow{t^o} 2CO_2 + H_2O\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH : x + 2y = \(\dfrac{60}{100} = 0,6(2)\)
Từ (1)(2) suy ra x = 0,1 ; y = 0,25
Vậy :
\(\%V_{CH_4} = \dfrac{0,1}{0,35}.100\% = 28,57\%\\ \%V_{C_2H_2} = 100\% - 28,57\% = 71,43\%\)

Đặt số mol CH4, C3H6, C2H2 trong m gam A là a, b, c mol
CH4 + 2O2 → CO2 + 2H2O
a 2a 2a
C3H6 + 4,5O2 → 3CO2 + 3H2O
b 4,5b 3b
C2H2 + 2,5O2 → 2CO2 + H2O
c 2,5c c
nO2 = 2a + 4,5b + 2,5c = 0,575 mol (1)
nH2O = 2a + 3b + c = 0,35 mol (2)
Đặt số mol CH4, C3H6, C2H2 trong 4,48 lít A là k.a, k.b, k.c mol
(hai phần có lượng khác nhau nhưng tỉ lệ giữa các chất trong hỗn hợp không đổi)
nA = ka + kb + kc = 0,2 mol
nBr2 = kb + 2kc = 0,25 mol
Lấy hai vế của phương trình chia cho nhau để triệt tiêu k
→ \(\dfrac{a +b+c}{b+2c}=\dfrac{0,2}{0,25}\) (3)
Từ (1), (2), (3)
→ a = 0,05, b = 0,05, c = 0,1

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
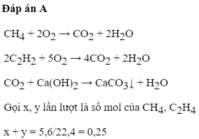
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
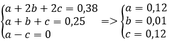
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

Đáp án A
Trong 33 gam X có : x mol CH4 ; y mol C2H2 ; z mol C3H6 ; ta có :
16x + 26y + 42z = 33 (1)
2x + y + 3z = 2,1 (2)
Trong 0,25 mol X thì có k.x mol CH4 ; ky mol C2H2 ; kz mol C3H6 Ta có :
kx + ky + kz = 0,25 (3) ; 2ky + kz = 0,3125 (4)
Lấy 3 chia 4 rút ra được x - 0,6y + 0,2z = 0 (5)
Từ (1) (2) (5) Giải ra được : x = 0,3 ; y = 0,6 ; z = 0,3
→ % thể tích C2H2 là : 0,6 : 1,2 = 50%
Đáp án A

Đáp án A
Trong 33 gam X có : x mol CH4 ; y mol C2H2 ; z mol C3H6 ; ta có :
16x + 26y + 42z = 33 (1)
2x + y + 3z = 2,1 (2)
Trong 0,25 mol X thì có k.x mol CH4 ; ky mol C2H2 ; kz mol C3H6 Ta có :
kx + ky + kz = 0,25 (3) ; 2ky + kz = 0,3125 (4)
Lấy 3 chia 4 rút ra được x - 0,6y + 0,2z = 0 (5)
Từ (1) (2) (5) Giải ra được : x = 0,3 ; y = 0,6 ; z = 0,3
→ % thể tích C2H2 là : 0,6 : 1,2 = 50%