Một bình đầy không khí ở điều kiện tiêu chuẩn , được đậy bằng một vật có khối lượng (2kg ). Tiết diện của miệng bình . Tìm nhiệt độ lớn nhất của không khí trong bình để không khí không đẩy được nắp bình lên và thoát ra ngoài. Biết áp suất khí quyển là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Ở điều kiện chuẩn p1 = 760 mmHg; ρ = 1,29 kg/m3.
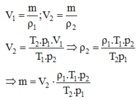
là khối lượng khí bơm vào bình sau nửa giờ.
khối lượng bơm vào sau mỗi giây:
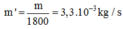

Chọn A.
Ở điều kiện chuẩn p 1 = 760 mmHg; ρ = 1,29 kg/ m 3 .


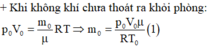
+ Khi không khí đà thoát ra khỏi phòng thì với lượng không khí còn lại trong phòng:


a, PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, Ta có: \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(V_{O_2}=18,48.\dfrac{1}{5}=3,696\left(l\right)\Rightarrow n_{O_2}=\dfrac{3,696}{22,4}=0,165\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{4}>\dfrac{0,165}{5}\), ta được P dư.
Theo PT: \(n_{P_2O_5}=\dfrac{2}{5}n_{O_2}=0,066\left(mol\right)\)
\(\Rightarrow m_{P_2O_5}=0,066.142=9,372\left(g\right)\)

Khi không khí chưa thoát ra khỏi phòng:
p 0 V 0 = m 0 μ R T ⇒ m 0 = p 0 V 0 μ R T 0 (1)
Khi không khí đã thoát ra khỏi phòng thì với lượng không khí còn lại trong phòng:
p 1 V 1 = m 1 μ R T ⇒ m 1 = p 1 V 1 μ R T 1 = p 1 V 0 μ R T 1 (2)
Từ (1) và (2)
⇒ m 1 = m 0 T 1 p 2 T 2 p 1 = ρ 0 V 0 T 0 p 1 T 1 p 0 ⇒ m 1 = 1 , 293.4.5.8 273.78 283.76 m 1 = 204 , 82 ( k g )
Thể tích khí thoát ra ở điều kiện chuẩn là:
Δ V 0 = Δ m ρ 0 = m 0 − m 1 ρ 0 ∆ V o = 206 , 88 − 204 , 82 1 , 293 = 1 , 59 m 3

C+O2to-->CO2
0,3--0,3--0,3
nC = 3,6 / 12 = 0,3 (mol)
=> VCO2(đktc) = 0,3 x 22,4 =6,72lít
=>Vkk=6,72\5=33,6l
PTHH: \(C+O_2\underrightarrow{t^o}CO_2\)
a) Ta có: \(n_C=\dfrac{3,6}{12}=0,3\left(mol\right)=n_{CO_2}\)
\(\Rightarrow V_{CO_2}=0,3\cdot22,4=6,72\left(l\right)\)
b) Theo PTHH: \(n_{O_2}=n_C=0,3mol\)
\(\Rightarrow V_{O_2}=6,72\left(l\right)\) \(\Rightarrow V_{kk}=6,72\cdot5=33,6\left(l\right)\)

Trạng thái 1: \(\left\{{}\begin{matrix}p_1=1atm\\V_1=11,2l\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái sau: \(\left\{{}\begin{matrix}p_2=1atm\\V_2=???\\T_2=0^oC=273K\end{matrix}\right.\)
Quá trình khí lí tưởng: \(\dfrac{p_1V_1}{T_1}=\dfrac{p_2V_2}{T_2}\)
\(\Rightarrow\dfrac{1\cdot11,2}{300}=\dfrac{1\cdot V_2}{273}\)
\(\Rightarrow V_2=10,192l\)

TK
Từ C2H4O2 ta có: M = 60 g/mol; mC = 2 x 12 = 24 g; mH = 4 x 1 = 4 g;
MO = 2 x 16 = 32 g.
%C = (24 : 60) x 100% = 40%; %H = (4 : 60) x 100% = 6,67%;
%O = 100% - 40% - 6,67% = 53,33%.
Đáp án: B
Ta có:
Lượng không khí trong bình được đun nóng trong một quá trình đẳng tích.
Trạng thái 1: t 1 = 0 0 C → T 1 = 0 + 273 = 273 K p 1 = 1 a t m
Trạng thái 2: t 2 = ? p 2 = F s + p 0
p 2 = p 0 + F s = 10 5 + 2.10 10.10 − 4 = 1,2.10 5 ( P a )
Trong quá trình đẳng tích:
p 2 T 2 = p 1 T 1 → T 2 = p 2 T 1 p 1 = 323,4 0 K