Cho hỗn hợp K2CO3 và NaHCO3 (tỉ lệ mol 1:1) vào bình đựng dung dịch Ba(HCO3)2 thu được kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 0,5M vào bình đến khi không còn khí thoát ra thì hết 560 ml. Biết toàn bộ Y phản ứng vừa đủ với 200 ml dung dịch NaOH 1M. Khối lượng kết tủa X là:
A. 3,94 gam
B. 7,88 gam
C. 11,28 gam
D. 9,85 gam


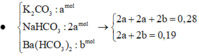

Đáp án B
Đặt n K 2 C O 3 = n N a H C O 3 = a mol; n B a ( H C O 3 ) 2 = b mol
Ta có phản ứng:
Ba2++ CO32-→BaCO3↓(∗)
b a mol
Khi cho HCl vào bình đến hết thoát khí, HCl sẽ phản ứng với BaCO3, NaHCO3, Ba(HCO3)2, K2CO3 có trong bình.
Ta có:
2H+ + CO32- → H2O + CO2
H+ + HCO3- → H2O + CO2
Ta có: ∑ n C O 3 2 - = a mol
∑ n H C O 3 - = a+2b mol
nHCl = nH+ = 0,56 × 0,5 = 0,28 mol
⇒ 2a + a + 2b = 0,28 (1)
Khi cho dung dịch Y tác dụng vừa đủ dung dịch NaOH, chỉ có HCO3- phản ứng.
HCO3- + OH- → H2O + CO32-
⇒ n H C O 3 - = n O H - ⇔ a + 2b = 0,2 (2)
Từ (1), (2) ⇒ a = 0,04; b = 0,08
Thế a, b vào phương trình (*)
⇒ m B a C O 3 =197×a =197×0,04 =7,88 g