Tỉ số nén là tỉ số giữa:
A. Thể tích toàn phần và thể tích công tác
B. Thể tích toàn phần và thể tích buồng cháy
C. Thể tích công tác và thể tích toàn phần
D. Thể tích buồng cháy và thể tích toàn phần
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Hướng dẫn
giả sử nA = 1 mol ; nC2H6 = x và nC2H2 = y; nH2O = nCO2 = 2 mol; x + y = 1 và 3x + y = 2 => x = 0,5 và y = 0,5 => %V = % số mol

Tham khảo:
Đốt cháy A chỉ tạo ra CO2 và H2O nên A chứa C;H;O
Vậy A có dạng CxHyOz
Phản ứng xảy ra:
CxHyOz+(x+y/4−z/2)O2to→xCO2+y2H2O
Ta có:
MA=1,4375MO2=1,4375.32=46
→12x+y+16z=46
Ta có:
nA=23/46=0,5 mol
nO2=33,6/22,4=1,5 mol
→x+y/4−z/2=nO2/nA=1,5/0,5=3
Ta có:
nCO2:nH2O=x:y2=2:3→x:y=2:6=1:3
Giải được: x=2;y=6;y=1
Vậy A là C2H6O

tham khảo
Diện tích hình trụDiện tích hình trụ gồm có diện tích xung quanh và diện tích toàn phần.
Diện tích xung quanh hình trụDiện tích xung quanh hình trụ chỉ bao gồm diện tích mặt xung quanh, bao quanh hình trụ, không gồm diện tích hai đáy.Công thức tính diện tích xung quanh bằng chu vi đường tròn đáy nhân với chiều cao.
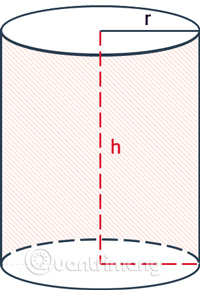 | Trong đó: Sxung quanh là diện tích xung quanh.r là bán kính hình trụ.h là chiều cao, khoảng cách giữa 2 đáy của hình trụ. |
Diện tích toàn phần được tính là độ lớn của toàn bộ không gian hình chiếm giữ, bao gồm cả diện tích xung quanh và diện tích hai đáy tròn.
Công thức tính diện tích toàn phần bằng diện tích xung quanh cộng với diện tích của 2 đáy
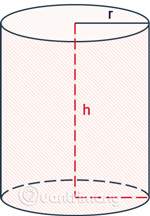 |

Khối lượng trung bình của 1 mol A :
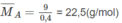
Trong hỗn hợp A phải có chất có M < 22,5 ; chất đó chỉ có thể là C H 4 .
Sau đó giải hệ 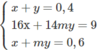
Ta tìm được m = 3; x = 0,3; y = 0,1.

1. Khi đun nóng A có mặt chất xúc tác Ni, chỉ còn lại 1 chất khí duy nhất. Vậy ankan và anken trong A có cùng số nguyên tử cacbon.
Giả sử trong 100 ml A có x mol C n H 2 n + 2 ; y mol C n H 2 n và z mol H 2 .
x + y + z = 100 (1)
Khi đốt cháy hoàn toàn 100 ml A :
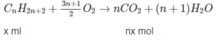
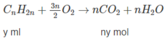
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 210 (2)
Khi đun nóng A có mặt chất xúc tác Ni:
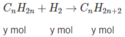
x + y = 70 (3)
y = z (4)
Giải hộ phương trình, tìm được n = 3; x = 40 ; y = z = 30.
Thành phần thể tích của hỗn hợp A là : C 3 H 8 : 40% ; C 3 H 6 : 30%; H 2 : 30%
2. Thể tích O 2 là 350 ml.

1. Anken và ankin có thể biến thành cùng một ankan, vậy 2 chất đó có cùng số nguyên tử cacbon. Giả sử 90 ml A có x mol C n H 2 n , y ml C n H 2 n - 2 , z ml H 2 .
x + y + z = 90 (1)
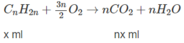
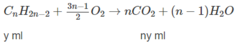
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 120 (2)
C n H 2 n + H 2 → C n H 2 n + 2
x ml x ml x ml
C n H 2 n - 2 + 2 H 2 → C n H 2 n + 2
y ml 2y ml y ml
H 2 đã phản ứng: x + 2y = z (3)
Thể tích ankan: x + y = 40 (4)
Giải hệ phương trình tìm được x = 30, y = 10, z = 50, n = 3
Hỗn hợp A: C 3 H 6 (33%); C 3 H 4 (11%); H 2 (56%).
2) Thể tích O 2 là 200 ml.

a, Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
Cho: nCO2 = 2 (mol), nH2O = 3 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 3 - 2 = 1 (mol)
Gọi CTPT cần tìm là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=2\)
Vậy: RH là C2H6.
b, Ở cùng điều kiện nhiệt độ, áp suất, tỉ lệ thể tích cũng là tỉ lệ số mol.
Cho nCO2 = 3 (mol), nH2O = 4 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 4 - 3 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=3\)
Vậy: CTPT cần tìm là C3H8.
c, Ta có: \(\dfrac{m_{CO_2}}{n_{H_2O}}=\dfrac{11}{9}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1}{2}\)
Cho nCO2 = 1 (mol), nH2O = 2 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 2 - 1 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=1\)
Vậy: CTPT cần tìm là CH4.
d, Ta có: \(\dfrac{m_{CO_2}}{n_{H_2O}}=\dfrac{44}{27}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)
Cho nCO2 = 2 (mol), nH2O = 3 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 3 - 2 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=2\)
Vậy: RH là C2H6.
e, Ta có: \(\dfrac{V_{H_2O}}{V_{CO_2}}=1,2\Rightarrow\dfrac{n_{H_2O}}{n_{CO_2}}=1,2=\dfrac{6}{5}\)
Cho nCO2 = 5 (mol), nH2O = 6 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 6 - 5 = 1 (mol)
Gọi CTPT của RH là CnH2n+2
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=5\)
Vậy: CTPT cần tìm là C5H12
Chọn B