Cho hỗn hợp MgO và MgCO3 tác dụng với dd HCl 20% thì thu được 6,72 lít khí (đktc) và 38 gam muối . Thành phần phần trăm của MgO và MgCo3 là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: nMgCl2=\(\dfrac{38}{95}\)=0,4(mol);
nCO2=\(\dfrac{6,72}{22,4}\)=0,3(mol)
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
(mol) 0,3 ← 0,3 ← 0,3
MgO + 2HCl → MgCl2 + H2O
(mol) 0,1 ← 0,1
\(\left\{{}\begin{matrix}mMgO=0,1.40=4g\\mMgCO3=0,3.84=25,2\end{matrix}\right.\)
=>%mMgO=\(\dfrac{4}{29,2}\).100=13,7%
=>%m MgCO4=86,3%

a/ \(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\)
\(0,5---0,5----0,5---0,5-0,5\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(b---b----b-----b\)
\(\Rightarrow m_{MgCO_3}=0,5.\left(24+12+16.3\right)=42\left(g\right)\)
\(\dfrac{m_{MgCO_3}}{m_{MgO}}=\dfrac{7}{3}\Rightarrow m_{MgO}=42.\dfrac{3}{7}=18\left(g\right)\Rightarrow n_{MgO}=b=0,45\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4}=0,45+0,5=0,95\left(mol\right)\) \(\Rightarrow m_{dd}=\dfrac{0,95.98}{0,05}=1862\left(g\right)\)

a)
\(n_{MgCl_2}=\dfrac{38}{95}=0,4\left(mol\right)\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: MgCO3 + 2HCl --> MgCl2 + CO2 + H2O
0,3<------0,6<------0,3<----0,3
MgO + 2HCl --> MgCl2 + H2O
0,1<---0,2<------0,1
=> \(\left\{{}\begin{matrix}m_{MgO}=0,1.40=4\left(g\right)\\m_{MgCO_3}=0,3.84=25,2\left(g\right)\end{matrix}\right.\)
b) \(m_{HCl}=\left(0,6+0,2\right).36,5=29,2\left(g\right)\)
=> \(m_{dd.HCl}=\dfrac{29,2.100}{20}=146\left(g\right)\)

\(a.PTHH:\)
\(Mg+2HCl--->MgCl_2+H_2\uparrow\left(1\right)\)
\(MgO+2HCl--->MgCl_2+H_2O\left(2\right)\)
b. ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT(1): \(n_{Mg}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{MgO}=12-0,2.24=7,2\left(g\right)\)
\(\Rightarrow\%_{MgO}=\dfrac{7,2}{12}.100\%=60\%\)
c. Ta có: \(n_{hh}=0,2+\dfrac{7,2}{40}=0,38\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_{hh}=2.0,38=0,76\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,76.36,5=27,74\left(g\right)\)
\(\Rightarrow m_{dd_{HCl}}=138,7\left(g\right)\)
\(\Rightarrow V_{dd_{HCl}}=126\left(ml\right)\)

Gọi \(\left\{{}\begin{matrix}n_{H_2}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{4,704}{22,4}=0,21\\\overline{M}=\dfrac{2a+44b}{a+b}=12,5.2=25\end{matrix}\right.\)
=> a = 0,095 (mol); b = 0,115 (mol)
Đặt nHCl = x (mol)
\(n_{MgCl_2}=\dfrac{12,825}{95}=0,135\left(mol\right)\)
Bảo toàn Cl: \(n_{CaCl_2}=\dfrac{x-0,27}{2}\left(mol\right)\)
Bảo toàn H: \(n_{H_2O}=\dfrac{x-2.0,095}{2}=\dfrac{x-0,19}{2}\left(mol\right)\)
BTKL:
\(m_{hh\left(bđ\right)}+m_{HCl}=m_{MgCl_2}+m_{CaCl_2}+m_{H_2}+m_{CO_2}+m_{H_2O}\)
=> \(19,02+36,5x=12,825+\dfrac{x-0,27}{2}.111+0,095.2+0,115.44+\dfrac{x-0,19}{2}.18\)
=> x = 0,63 (mol)
=> \(n_{CaCl_2}=0,18\left(mol\right)\)
=> mCaCl2 = 0,18.111 = 19,98 (g)

Đáp án A
n khí = 0,42 mol
nMgCl2 = 0,27 mol
Quy đổi hỗn hợp đầu về: Ca (x mol), Mg (0,27 mol), C (0,23 mol), O (y mol)
m hỗn hợp = 40x+0,27.24+0,23.12+16y = 38,04 (1)
BT e: 2nCa + 2nMg + 4nC = 2nO + 2nH2 => 2x + 0,27.2 + 0,23.4 = 2y + 0,19.2 (2)
Giải (1) và (2) => x = 0,36; y = 0,9
=> mCaCl2 = 0,36.111 = 39,96 gam

Giải thích:
n khí = 0,42 mol
nMgCl2 = 0,27 mol
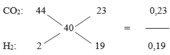
CO2: 44 23 0,23
25 =
H2: 2 19 0,19
Quy đổi hỗn hợp đầu về: Ca (x mol), Mg (0,27 mol), C (0,23 mol), O (y mol)
m hỗn hợp = 40x+0,27.24+0,23.12+16y = 38,04 (1)
BT e: 2nCa + 2nMg + 4nC = 2nO + 2nH2 => 2x + 0,27.2 + 0,23.4 = 2y + 0,19.2 (2)
Giải (1) và (2) => x = 0,36; y = 0,9
=> mCaCl2 = 0,36.111 = 39,96 gam
Đáp án A
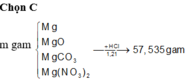
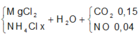

MgO + 2 HCl -> MgCl2 + H2O
x______2x_____x_______x(mol)
MgCO3 + 2 HCl -> MgCl2 + CO2 + H2O
y___2y__________y______y(mol)
nMgCl2= 38/95=0,4(mol)
nCO2= 6,72/22,4= 0,3(mol)
\(\left\{{}\begin{matrix}y=0,3\\x+y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,3\end{matrix}\right.\)
=> mMgO= 40.0,1=4(g)
mMgCO3= 0,3. 84= 25,2(g)
=> \(\%mMgO=\frac{4}{4+25,2}.100\approx13,699\%\\ \rightarrow\%mMgCO3\approx100\%-13,699\%\approx86,301\%\)
\(\left\{{}\begin{matrix}MgO\\MgCO_3\end{matrix}\right.+HCl\rightarrow\left\{{}\begin{matrix}MgCl_2+H_2O\left(1\right)\\MgCl_2+H_2O+CO_2\left(2\right)\end{matrix}\right.\)
Ta có: \(n_{MgCl_2}=0,4\left(mol\right)\)
\(n_{CO_2}=0,3\left(mol\right)\)
\(\Rightarrow n_{MgCO_3}=n_{MgCl_2\left(2\right)}=0,3\left(mol\right)\)
\(\Rightarrow n_{MgO}=n_{MgCl_2\left(1\right)}=0,1\left(mol\right)\)
\(\Rightarrow\%m_{MgO}=\frac{0,1.40}{0,1.40+0,3.84}.100\%=13,99\text{%}\)
\(\%m_{MgCO_3}=86,01\%\)
Bạn than khảo nhé!