Bài 4: Đốt cháy hoàn toàn a gam hỗn hợp X gồm etilen, propilen và but-1-en cần dùng vừa đủ b
lít O2 (đktc) thu được 2,4 mol CO2. Tìm giá trị b.
Bài 5: Đốt cháy hoàn toàn 0,2 mol hỗn hợp 2 hiđrocacbon A, B (đều mạch hở) có khối lượng mol
hơn kém nhau 14 đơn vị thì thu được 15,68 lít CO2 (đktc) và 12,6 g H2O. Xác định CTPT của A
và B và thành phần % về số mol mỗi chất trong hỗn hợp.
Bài 6: Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm hai anken kế tiếp nhau trong dãy đồng đẳng
thu được khí CO2 và hơi nước có khối lượng hơn kém nhau 6,76 gam. Xác định CTPT của 2
anken.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Áp dụng định luật bảo toàn nguyên tố O có 2nO2 = 2nCO2 + nH2O
⇒ nO2 = (2,4.2 + 2,4 )/2 = 3,6 ⇒ b = 3,6.22,4 =80,64l
Đáp án C.

Đáp án C
a gam hh C2H4, C3H6, C4H8 + b lít O2 → 2,4 mol CO2 + 2,4 mol H2O
Theo bảo toàn nguyên tố O: nO2 = (2 x nCO2 + 1 x nH2O) : 2 = (2 x 2,4 + 2,4) : 2 = 3,6 mol
→ b = 3,6 x 22,4 = 80,64 lít

Đáp án C
Hướng dẫn
CnH2n + 3n/2O2 → nCO2 + nH2O
nO2 = 3/2 n CO2 = 3/2 . 2,4 = 3,6 mol => VO2 = 3,6.22,4 = 80,64 lít

Đáp án C
Hướng dẫn CnH2n + 3n/2O2 → nCO2 + nH2O
nO2 = 3/2 nCO2 = 3/2.2,4 = 3,6 mol => VO2 = 3,6.22,4 = 80,64 lít

Chọn đáp án C.
X gồm: OHC-CHO, C2H2, CH2(CHO)2, HCOOCH=CH2.
CTPT các chất là: C2H2O2, C2H2, C3H4O3.
n
C
2
H
2
O
2
=
n
C
2
H
2
Áp dụng định luật bảo toàn nguyên tố O có:
x
+
2
y
+
2
n
O
2
=
x
+
2
y
+
2.
52
,
8
44
⇒
n
O
2
=
1
,
2
m
o
l
0,12 mol (C2H6, C3H8) + 0,546 mol O2 → a g CO2
Có n H 2 O − n C O 2 = n a n k a n = 0 , 12 m o l (1)
Áp dụng định luật bảo toàn nguyên tố O: n H 2 O = 2.0 , 546 − 2 n C O 2 (2)
Từ (1), (2) suy ra n C O 2 = 0 , 324 m o l ⇒ a = 44.0 , 324 = 14 , 256 g n H 2 O = 0 , 444 m o l

- Bảo toàn nguyên tố O ta có:
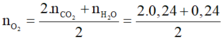
= 0,36(mol)
- Vậy b = 0,36.22,4 = 8,064 lít.
- Chọn đáp án C.
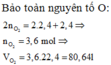

Câu 1 :
Ta có hh đều là các anken nên nCO2=nH20=2,4mol
Bảo toàn ng tố Oxi ta có:\(2n_{O2}+2n_{CO2}+n_{H2O}\)
\(2n_{O2}=2,4.2+2,4\)
\(\Rightarrow n_{O2}=3,6\left(mol\right)\)
\(\Rightarrow V_{O2}=3,6.22,4=80,64\left(l\right)\)
Câu 2:
\(n_{CO2}=0,7\left(mol\right),n_{H2O}=0,7\left(mol\right)\)
Do nCO2 = nH2O nên hidrocacbon A và B là anken
Số C trung bình\(=\frac{n_{CO2}}{n_{hh}}=\frac{0,7}{0,2}=3,5\)
3 < 3,5 < 4 nên CTPT của A và B lần lượt là C3H6 và C4H8
Câu 3:
Ta có
X là anken nên nCO2=nH2O
Gọi a là nCO2
Ta có
\(44a-18a=6,76\Rightarrow a=0,26\left(mol\right)\)
\(\Rightarrow n_{CO2}=n_{H2O}=0,26\left(mol\right)\)
Số C trung bình \(=\frac{0,26}{0,1}=2,6\)
Vậy 2 anken là C2H4 và C3H6
Phần 2 (Bài 5)
Gọi a là số mol C3H6 b là số mol C4H8
Ta có
\(\left\{{}\begin{matrix}a+b=0,2\\3a+4b=0,7\end{matrix}\right.\Rightarrow a=b=0,1\)
\(\%V_{C3H6}=\%V_{C4H8}=50\%\)